药事日报313期 | 受集采影响总市值跌破千亿关口?多项药物临床进度更新
时间:2022/01/19来源:医药之梯阅读:454
诗迈·药事日报 | NO.313期 |
欢迎来到本期药事日报 及时医药界资讯一手掌握!!! |本期内容速览| ● 一线治疗肝癌!双重免疫组合疗法降低死亡风险22% ● III期临床曾被终止 罗氏即将再度启动ASO新药临床试验 ● IL-17A/F***达到3期临床主要终点 ● 创新血检获FDA突破性医疗器械认定 ● 瓴路药业任张晓雷为CEO John Maraganore、Peter Ho为战略顾问 ● 长春高新跳水跌停 总市值跌破千亿关口 ● 之江生物四款新冠检测试剂盒获欧盟CE认证 01 一线治疗肝癌! 双重免疫组合疗法降低死亡风险22% 今日,阿斯利康(AstraZeneca)公司宣布,重磅PD-L1***度伐利尤单抗(durvalumab,英文商品名:Imfinzi)与抗CTLA-4抗体tremelimumab联用,在一线治疗不可切除的肝细胞癌患者的3期临床试验中与活性对照相比,显著延长患者的总生存期。 Imfinzi是一款抗PD-L1单克隆抗体,通过阻断PD-L1与PD-1和CD80蛋白的结合,解除肿瘤细胞对免疫反应的抑制。它已经在多个国家和地区获得批准治疗广泛期小细胞肺癌。并且获得FDA批准治疗非小细胞肺癌和晚期膀胱癌。 Tremelimumab阻断CTLA-4的活性,从而促进T细胞激活,激发免疫系统对癌症的免疫反应。它与Imfinzi和化疗联用,在一线治疗IV期非小细胞肺癌的3期临床试验中显著改善患者的总生存期。 来源:阿斯利康 02 III期临床曾被终止,罗氏即将再度启动ASO新药临床试验 1月18日,Ionis公司宣布其合作伙伴罗氏制药正在设计一项新的2期临床,以评估反义寡核苷酸(ASO)药物tominersen(研发代号:IONIS-HTTRx,RG6042/RO7234292)在亨廷顿病(HD)中的疗效。 来自:Ionis官网 此前在2021年3月,基于3期临床GENERATIONHD1中该药的潜在风险/收益比缺乏优势,罗氏终止了该项临床的患者给药。在中国,RG6042也已于2020年登记启动临床试验,当前状态为「主动终止」。不过该研究仍在进行中,无需给药,以使参与者能够被跟踪以了解安全性和临床结果,按计划将于2022年3-4月在最后一名患者最后一次就诊时完成。 来源:Insight数据库 03 IL-17A/F***达到3期临床主要终点 2022年1月18日,优时比(UCB)公司宣布了抗IL-17A/F抗体Bimzelx(bimekizumab)的一项3期临床试验的积极中期分析结果。试验达到其主要终点和所有重要次要终点,表明bimekizumab能有效改善活动性非放射学中轴型脊柱关节炎(nr-axSpA)成人患者的临床症状。 这项试验与该药在强直性脊柱炎患者中开展的另一项试验,共同证明了bimekizumab在整个疾病谱系中的治疗潜力。基于获得的数据,优时比计划在今年第三季度提交bimekizumab治疗中轴型脊柱关节炎(axSpA)的监管申请。 axSpA是影响骨盆关节和脊柱的一种脊柱关节炎,可表现为慢性炎症性背痛,脊柱僵硬,骨骼功能和活动能力受损。全世界约有450万成年axSpA患者。根据X光放射学检测能否发现骶髂关节的损伤,患者可分为非放射学中轴性脊柱关节炎(nr-axSpA)和r-axSpA两类。axSpA的总患病率在成人中约为0.2%~1.4%,约一半是nr-axSpA患者,10%~40%的nr-axSpA患者在2~10年内进展为强直性脊柱炎。 来源:优时比(UCB)公司 04 创新血检获FDA突破性医疗器械认定 Diadem公司今天宣布,美国FDA已授予AlzoSure Predict检测突破性医疗器械资格(Breakthrough Device Designation),这是Diadem基于血液的生物标志物的预后检测方法,旨在高精度地识别50岁以上有认知障碍迹象的个体在症状明显之前是否会进展为阿尔茨海默病。新闻稿指出,这一检测可提前6年判定疾病是否会进展为阿尔茨海默病。 突破性医疗器械认定被授予有可能对危及生命或不可逆衰弱性疾病提供更有效诊断或治疗的新型医疗器械。突破性医疗器械认定让研发公司在开发过程中获得美国FDA额外的指导,以及对上市申请的加速审评。 Diadem正在开发的AlzoSure Predict检测试剂盒是一种简单、非侵入性的基于血浆生物标志物的检测试剂盒。该公司的分析方法包括其开发的一种专有抗体,旨在与U-p53AZ结合。U-p53AZ是p53蛋白的构象变体,在多项研究中与阿尔茨海默病的发病机制有关。 来源:药明康德 05 瓴路药业任张晓雷为CEO 近日,瓴路药业宣布任命联合创始人张晓雷为全职首席执行官;张晓雷(MBA)自2021年5月起担任瓴路临任首席执行官。 此外,瓴路还任命Alnylam前创始人兼首席执行官John Maraganore博士和百济神州联合创始人兼前总裁Peter Ho博士为公司的战略顾问。 来源:瓴路药业 06 信达生物与Amagma合作开发3款酶靶向抗体药 2022年1月18日,信达生物与Amagma Therapeutics达成合作协议,开发至多3款酶特异性的抗体药物。信达生物拥有大中华区权益,Amagma保有中国外全球权益。信达生物支付一定的预付款、里程碑金额以及销售分成。 酶参与了许多生理、病理过程,Amagma Therapeutics聚焦于针对酶靶点,开发特异性抗体药物,建立了相应的SEIZMIC技术平台。 Amagma Therapeutics的技术核心体现在自主的酶设计、表达和纯化能力,独特的体内、体外酶测试方法以及抗体发现和优化平台。在此技术基础上,Amagma建立了一系列研发管线,首个产品将于2023年进入临床阶段。 来源:信达生物 07 长春高新跳水跌停 总市值跌破千亿关口 1月19日,广东省药品交易中心发布公告称,为满足医疗机构药品采购需求,促进药品形成合理市场价格,按照 《广东省医疗保障局关于做好药品和医用耗材采购工作的指导意见》 (粤医保规〔2020〕2 号)的精神,省药交中心开展双氯芬酸等276个药品联盟地区集中带量采购工作,现邀请符合要求的企业前来申报。 来源:新浪医药新闻 08 之江生物四款新冠检测试剂盒获欧盟CE认证 1月19日,之江生物发布公告称,公司产品新型冠状**抗原检测试剂盒(胶体金法)、新型冠状**中和抗体检测试剂盒(ELISA)、新型冠状**中和抗体检测试剂盒(胶体金法)、新型冠状**(SARS-CoV-2)L452R &P681R 突变检测试剂盒于近期获得四项欧盟CE认证,有效期到2025年5月26日。 来源:之江生物



最新医药动态
更多»相关资讯
更多»- 1精准医疗的技术基础—分子诊断技术发展现状
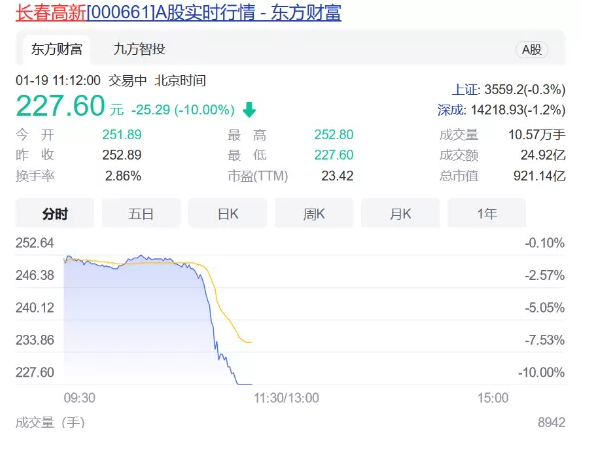
- 2药事日报|国内首个重组抗狂犬病毒单抗药物申报上市、药企最新排行榜公布、大流行中新冠病毒D614G普遍突变感染滴度最大增加近十倍
- 3海思科创新抗肿瘤小分子药物IND申请获受理
- 42019年仿制药获批最大赢家——正大天晴
- 5国家药监局发布上市药品临床安全性文献评价指导原则
- 6最新医保药品目录调整方案敲定:这些药不在考虑范围
- 7药事日报130期|辅仁药业财务造假被罚590万元 实控人朱文臣10年市场禁入、前沿生物正式在科创板上市
- 84+7扩围在即 药店又该如何应对?
- 9关于公示广州白云山天心制药股份有限公司注射用头孢呋辛钠限价的通知
- 10创业公司失去创始人会怎么样?创始人死于30月前
- 11谁来打破IVD企业的IPO“魔咒”?
- 12药事日报278期 |重磅!贝达药业贝伐珠单抗注射液获批上市
- 13为什么说这次药品集采把价格水分都去掉了?
- 14药事日报163期|Henri Nico Doods博士出任和其瑞医药总裁及临床研发负责人、埃及正与中国谈判新冠疫苗的生产
- 15川药械采〔2017〕9号关于公布2015年四川省公立医院药品集中采购第一阶段谈判(议价)结果的通知
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
