药事日报329期 | 传奇生物临床试验遭叫停!多家药企高层人事变动!

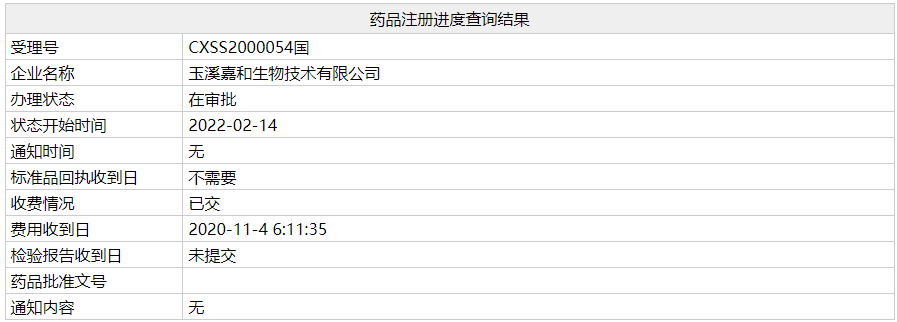
步长制药注销全资子公司中欣顺发 2月16日,步长制药发布公告称,公司根据目前的实际经营情况及后续业务发展规划,为优化资源配置及组织结构,降低管理成本,提高运营管理效率,决定对其全资子公司中欣顺发予以注销。 本次注销事项不涉及关联交易,亦不构成《上市公司重大资产重组管理办法》规定的重大资产重组,无需提交董事会、股东大会批准。 上述事项已办理完毕,公司近日收到咸阳市市场监督管理局出具的《外商投资企业注销登记通知书》。 来源:步长制药 传奇生物一项CAR-T疗法临床试验遭FDA叫停 近日,根据国外生物制药网站Fierce Pharma的报道,美国FDA通知传奇生物一项临床暂停,并将于3月11日前提供正式的临床暂停函。 此次临床暂停涉及传奇生物的一款早期CAR-T细胞疗法,该疗法在去年才刚刚启动1期临床试验。现在,FDA已通知该公司停止。 传奇生物在周二上午的一份简短新闻稿中宣布了LB1901的临床暂停。在收到FDA的临床暂停通知之前,该公司在对第一例患者给药并出现CD4+T细胞计数低后已自愿暂停试验。 根据传奇生物的说法,该患者没有经历任何与药物相关的严重不良事件,正在接受监测。 来源:一度医药 信达PCSK9单抗3期临床达到终点,拟报上市 2月17日,信达生物宣布,公司自主研发的重组全人源抗前蛋白转化酶枯草溶菌素9(PCSK-9)单克隆抗体(研发代号:IBI306)的两项中国关键注册临床研究——CREDIT-1 研究(治疗非家族性高胆固醇血症 [non-FH] 合并高危/极高危心血管风险)和 CREDIT-4 研究(治疗非家族性高胆固醇血症 [non-FH] 和杂合子型家族性高胆固醇血症 [HeFH]),均达到主要研究终点。CREDIT-1 和 CREDIT-4 相关研究结果将在未来的国际学术会议上予以公布。 截至目前,IBI306三项主要关键注册临床研究均已完成且均顺利达到主要研究终点,其中 CREDIT-2 研究(治疗杂合子型家族性高胆固醇血症 [HeFH])已于 2021 年 8 月达到临床终点。信达生物计划就递交 IBI306 用于原发性高胆固醇血症和混合型血脂异常的适应症上市申请与国家药品监督管理局药品审评中心(CDE)进行沟通。 IBI306是信达生物制药自主研发的创新生物药,IgG2全人源单克隆抗体,能特异性结合 PCSK-9 分子,通过减少 PCSK-9 介导的低密度脂蛋白受体(LDLR)内吞来增加 LDLR 水平,继而增加 LDL-C 清除,降低 LDL-C 水平。 来源:信达生物 第七批国采企业开始申报共涉及208个品规 2月17日,上海阳光医药采购网发布《关于开展第七批国家组织药品集中采购相关药品信息填报工作的通知》,自2022年2月18日起,联合采购办公室开展第七批国家组织药品集中采购相关药品信息填报工作。 此次国采共涉及208个品规,包括阿法替尼口服常释剂型、阿立哌唑口腔崩解片、昂丹司琼注射剂等。 (详情看今日文章) 来源:上海阳光医药采购网 嘉和生物「英夫利西单抗」即将获批 2月17日,NMPA官网显示,玉溪嘉和生物技术有限公司的英夫利西单抗生物类似药上市申请进度「在审批」阶段,有望在近日获得批准。如若获批,这将是国产第3款英夫利西单抗生物类似药。 英夫利西单抗是强生/默沙东研发的一款特异性阻断肿瘤坏死因子(TNF-α)的人鼠嵌合型单克隆抗体,可与TNF-α的可溶形式(sTNF-α)和跨膜形式(tmTNF-α)以高亲和力结合,抑制TNF-α与受体结合,从而使TNF失去生物活性。 该药于1998年首次获 FDA 批准在美国上市,次年在欧洲获批上市,2006年在国内获批上市,商品名为类克®。类克的峰值销售额达到 92.40亿美元,尽管已经受到生物类似药冲击,2020年仍实现40.77亿美元销售额。 来源: Insight 数据库 北海康成任命胡澜为**董事 2月17日,北海康成宣布委任胡澜博士为公司**非执行董事兼董事会薪酬委员会委员,自2022年2月16日起生效。 胡澜博士在医疗投资、运营及行政管理方面拥有广泛背景。她于2004年创办了北京美中宜和妇儿医院有限公司,担任该公司的董事长和总经理。目前,胡博士担任北京美中宜和医疗管理(集团)有限公司的董事长兼总经理、北京美中爱瑞肿医院有限责任公司董事长、北京医大时代科技发展有限公司**董事及北京轩和雅致管理咨询有限公司执行董事兼总经理。自2013年至今,胡博士还担任北京市第十二届及第十三届政协委员。此外,自2002年至2004年,胡博士还曾担任美国摩根大通投资银行经理。 胡澜博士自北京医科大学(现北京大学医学部)获得医学学士学位,自美国俄亥俄医科大学获得医学科学博士学位,并且自美国密歇根大学获得工商管理硕士学位。 来源:北海康成 药石科技任命顾震天为质量及注册高级副总裁 2月16日,药石科技宣布,公司于近日任命顾震天博士担任质量及注册高级副总裁,全面负责药石科技的质量管理和注册管理工作。 顾博士在新药研发领域拥有超过二十年的研发及管理经验,先后任职于美国宝洁(Proctor & Gamble)、葛兰素史克 (GlaxoSmithKline)、3M及赛诺万(Theravance)等公司。 在加入药石科技前,顾博士曾担任美国赛诺万(Theravance)分析研发及质量控制副总裁,负责创新药分析方法开发、验证、杂质鉴定及毒性水平认证、质量控制及药物代谢等方面的研发及管理工作。他带领Vibativ(注射用Telavancin)项目CMC团队完成了从临床II期到NDA申报和商业化阶段的关键工作;并负责Telavancin CMC部分在欧美,加拿大,俄罗斯及其他国家和地区的注册申报。 从1998年至今,顾博士领导或参与了超过十个创新药的临床开发项目,并已有五个药品获批上市,在美国、欧盟、中国以及全球多个法规市场积累了丰富的CMC方面的新药注册申报经验。 来源:奥赛康药业 又有3名患者死亡!渤健阿尔茨海默病药Aduhelm争议不断 Aduhelm自推出以来,一直备受争议,日前又有3名接受渤健Aduhelm治疗的阿尔茨海默病患者不幸死亡。尽管目前还没有确定几名患者具体的死亡原因,不过这一消息也使得外界再一次关注这款争议药物潜在的安全性风险。 这些死亡案例是通过美国FDA**的不良事件报告系统FAERS登记的,此外,数据库中还包含Aduhelm导致的淀粉样蛋白相关成像异常(ARIA)的副作用报告。加拿大皇家银行资本(RBC)分析师在分析了此前1名Aduhelm患者的死亡报告后表示,患者出现的ARIA“很可能就是由于Aduhelm治疗造成的”。RBC在周三给投资者的一份报告中也特别强调了这一信息,分析师Brian Abrahams写道,“这些患者死亡案例是否与Aduhelm治疗有关,或者只是偶然事件,目前仍然难以区分。” 此次3名死亡案例中,其中1名死亡患者的年龄为86岁,伴发糖尿病和心脏病,而另一名患者74岁,伴发步态障碍,第三名患者的年龄未知,三名患者均因癫痫发作而接受治疗,但渤健并没有具体说明患者死亡是否与ARIA有关。RBC分析师对此表示,仅去年第四季度,427名接受Aduhelm治疗的患者中就至少有3人死亡,该疗法潜在的治疗风险“值得密切关注”。 然而,渤健则批驳了这一观点,称迄今为止报告的“死亡病例均与Aduhelm治疗无关”。该公司发言人表示,阿尔茨海默症是一种非常复杂的疾病,患者经常患有其他严重疾病,暗示患者是死于其他疾病。渤健对RBC报告中提出的论点也提出质疑,表示虽然在Aduhelm治疗试验期间确实发生了严重的ARIA事件,但大多数副反应程度属于“轻度或中度”,且通常发生在治疗过程的早期阶段,患者往往可以自行缓解并且在临床上也在可控的范围内。渤健表示该公司在试验中已经在大多数ARIA副反应发生的时期(Aduhelm前8剂治疗期间),加强了针对ARIA副反应的检测和管理计划。 (原文删减) 来源:一度医药