药事日报360期 | 原赛诺菲中国首席市场官周游加入基石药业!Longeveron股价暴涨105%?!
时间:2022/04/01来源:医药之梯阅读:470

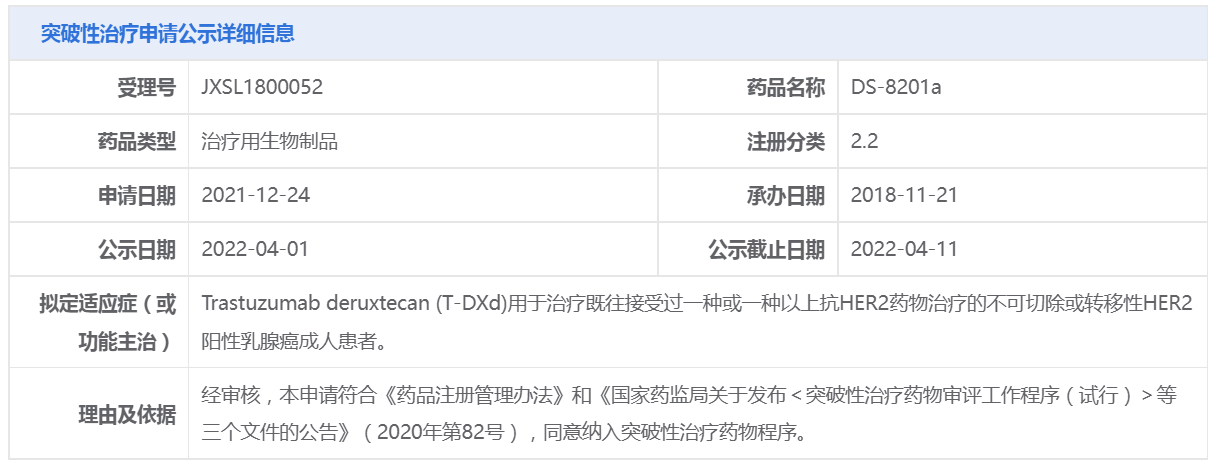
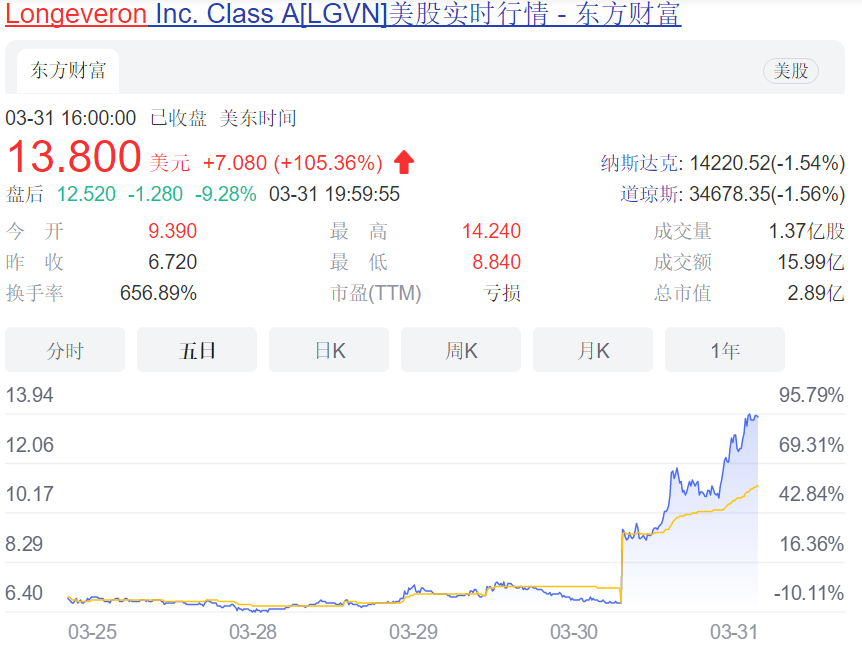
亿帆医药:FDA将推迟F-627上市申请批复 3月31日,亿帆医药发布关于控股子公司在研产品F-627项目的进展公告。 公告显示,亿帆医药控股子公司EviveBiotechLtd.在研产品艾贝格司亭α注射液(以下简称“F-627”)用于预防及治疗肿瘤患者在化疗过程中引起的嗜中性粒细胞减少症于2022年3月31日(美国时间2022年3月30日)收到美国FDA的邮件通知,因旅行限制,FDA将推迟F-627上市申请批复,直到现场检查完成。 22021年3月30日,公司控股子公司亿一生物向美国FDA提交了F-627生物制品许可申请(BLA),并于2021年5月27日收到FDA的受理函,约定F-627审批目标日期为2022年3月30日。 FDA通知具体内容:“在**提交的F-627申请时,我们就明确FDA批准F-627上市申请前,需对亿一生物制药(北京)有限公司进行现场检查,以评判其是否具有符合cGMP要求的生产能力。但目前由于旅行限制,我们无法在当前**周期内对亿一生物制药(北京)有限公司进行现场检查,因此,FDA将延期F-627上市申请的批复,直至完成现场检查。我们也将持续关注公共卫生形势及旅行限制政策,一旦安全旅行得以恢复,并在公共卫生和其他因素允许的情形下,我们将积极明确一种方法,以完成目前尚未完成的现场检查。” 亿帆医药表示,截止目前公司控股子公司亿一生物就FDA对F-627技术审评过程中提出的问题均全部回复。本次控股子公司收到FDA因旅行限制无法对子公司进行生产现场检查,推迟F-627上市申请批复的通知,并非F-627项目本身导致的延期。公司将积极做好生产现场核查前的准备工作,随时迎接FDA的现场检查,竭力推进F-627尽快上市。但F-627生产现场检查时间及结果尚不确定,F-627能否最终获批上市仍存在不确定性。 来源:亿帆医药 治疗乳腺癌,第一三共ADC药物拟纳入突破性治疗品种 4月1日,CDE官网最新显示,第一三共ADC药物Trastuzumab deruxtecan(T-DXd)拟纳入突破性治疗品种,用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性乳腺癌成人患者。 T-DXd是一种新型抗HER2靶向抗体偶联药物(ADC),以第一三共原研独创的DXd ADC技术为依托,由人源化抗HER2 lgG1抗体、可裂解的四肽连接子和拓扑异构酶I***(喜树碱衍生物DXd)组成,具备精准靶向和高效低毒的双重优势,此前T-DXd已在全球多个国家获批应用,并获得四项美国食品药品监督管理局(FDA)授予的突破性疗法认定。 此前,T-DXd曾获CDE突破性疗法资格,单药用于既往接受过一种或一种以上治疗方案的HER2阳性局部晚期或转移性胃或食管胃结合部(GEJ)腺癌成人患者的治疗。 来源:CDE官网 阿尔茨海默症新药I期结果发表,Longeveron股价暴涨105% 3月31日,Longeveron宣布,阿尔茨海默症协会(Alzheimer 's & Dementia®)杂志发表了一项针对轻度阿尔茨海默症(AD)患者的I期试验结果。该试验达到了主要终点,表明Lomecel-B在该患者群体中具有良好的耐受性。此外,这些数据支持进一步探索Lomecel-B的疗效,特别是在减缓AD患者认知功能下降和改善生活质量方面的治疗潜力。 受此消息影响,该公司股价上涨105%。 来源:医药魔方 假冒HIV药物肆虐,美国***对相关药品展开调查 近日,由于Biktarvy、Descovy和Symtuza等抗**病(HIV)药的假冒药物肆虐,美国***展开针对吉利德、葛兰素史克和强生假冒药物的调查,力求清除流通系统中危及患者健康和治疗的伪劣药物。 Biktarvy和Descovy均为吉利德旗下的抗**病药物。其中,Biktarvy是一种治疗HIV/AIDS的抗逆转录**鸡尾酒疗法,由三种固定剂量的药物组成,2020年,该药物的销售额达86亿美元。而Descovy用于HIV暴露前防护,2020年销售额为17亿美元。 抗****药物通常由医疗保险和医疗补助以低成本或免费提供给有需要的患者,制造商通过从无家可归或**成瘾的**病患者手中购买药物,并虚假转售给药店。服用Biktarvy患者每月需要花费3751美元,而强生Symtuza的药价更甚,为4490美元/月。高药价使转售对造假者、药店和患者都具有很大的诱惑力。 目前美国***已经介入调查并与相关公司和FDA合力清除所有假冒药品。据悉,马里兰州的批发分销商Safe Chain Solutions是吉利德起诉的被告之一,但该公司表示其从未故意销售过假冒产品。 (原文有删减) 来源:一度医药 显著改善帕金森病患者症状,新机制疗法2期临床结果积极 今日,Cerevance公司宣布,其潜在“first-in-class”口服帕金森病在研疗法CVN424在2期临床试验中获得积极结果。在达到安全性目标之外,CVN424为患者的“OFF”期提供了统计显著且具有临床意义的剂量依赖性改善。“OFF”期指的是患者即使接受治疗后依然出现帕金森病症状的时间段。 Cerevance公司的药物发现平台基于名为NETSseq的新技术,它可以从患者大脑组织中标记并且收集特定与疾病相关的细胞类型,然后对其进行转录子组和表观遗传学分析,基于这些知识发现治疗中枢神经系统疾病的新靶点。CVN424是基于这一平台发现的创新疗法,它选择性靶向与帕金森病相关的多巴胺D2受体依赖性间接信号通路,旨在产生和左旋多巴或脑深部刺激相同的积极效果的同时,避免不良反应。 在这项随机双盲,含安慰剂对照的2期临床试验中,约135名帕金森病患者接受了两种不同剂量的CVN424的治疗。他们稳定接受左旋多巴或其它帕金森病药物的治疗,但是每天仍然有至少两个小时的“OFF”期。 试验结果显示,接受治疗4周后,与安慰剂相比,高剂量CVN424将“OFF”期改善1.3个小时(p=0.042)。与此同时,无运动障碍的“ON”时间增加。与其它和左旋多巴同时使用的辅助疗法不同,CVN424与安慰剂相比,降低患者的白天嗜睡指标。 来源:药明康德 维力医疗副总经理黄岸辞职 3月31日晚间,维力医疗发布公告,公司董事会于近日收到公司副总经理黄岸的书面辞职报告,黄岸因工作调整原因申请辞去公司副总经理职务。 黄岸的辞职报告自送达公司董事会之日起生效,辞去公司副总经理职务后,将在公司控股子公司广州维力健益医疗器械有限公司担任管理职务,其辞去公司副总经理职务不会对公司生产经营产生任何影响。 来源:维力医疗 原赛诺菲中国首席市场官周游加入基石药业 4月1日,基石药业任命周游博士为公司大中华区总经理兼公司商业部负责人,全面负责公司产品商业化工作,向基石药业董事长兼首席执行官江宁军博士直接汇报。 据了解,加入基石药业之前,周游曾任赛诺菲巴斯德(中国)首席市场官。 来源:基石药业
最新医药动态
更多»相关资讯
更多»- 1美国FDA批准Ionis-AstraZeneca的神经疾病药物
- 2罗氏2019年业绩:国际制药业务增长11% 中国市场功不可没
- 3CAR-T疗法中国商业化将至,差异化竞争何以为营?
- 4川药采联办〔2017〕3号关于停止部分药品上网采购并给予不良记录的通知
- 5药事日报97期|海思科与海创药业合作终止2.6亿转让专利、西藏药业3.5亿元获斯微生物疫苗权益后再投3.4亿元建生产线
- 6康哲应战做空!最大CSO悄然掌控全产业
- 72019年仿制药获批最大赢家——正大天晴
- 812亿元!医药反腐又爆大瓜?
- 9药事日报439期 | 科越医药新高层任命!吉利德2022H1发布!全球CRO“一哥”分拆业务独立上市!
- 10医药快讯丨朗视仪器终止科创板IPO;广药集团与外泌体行业新锐安龄生物达成战略合作
- 11药事日报405期 | 赛生药业、帕母医疗等最新人事变动;辉瑞JAK新药在国内开售;北京涉酒吧疫情已判定密接6158人!
- 1220万国人数据:50%心脏代谢病死亡都是没吃对!
- 13(2017)6号关于硫酸镁注射液和重酒石酸间羟胺注射液临床紧缺药品挂网采购的通知
- 142019哈尔滨瀚邦医疗科技有限公司最新招聘信息
- 15药事日报450期 | 41亿美元!BMS收购Turning Point;叮当健康通过港交所聆讯,预计将于近期上市
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
