药事日报376期 | 由盈转亏!天士力2022年Q1净亏损5.57亿元!国药集团中国生物奥株新冠病毒灭活疫苗获批
时间:2022/04/26来源:医药之梯阅读:425

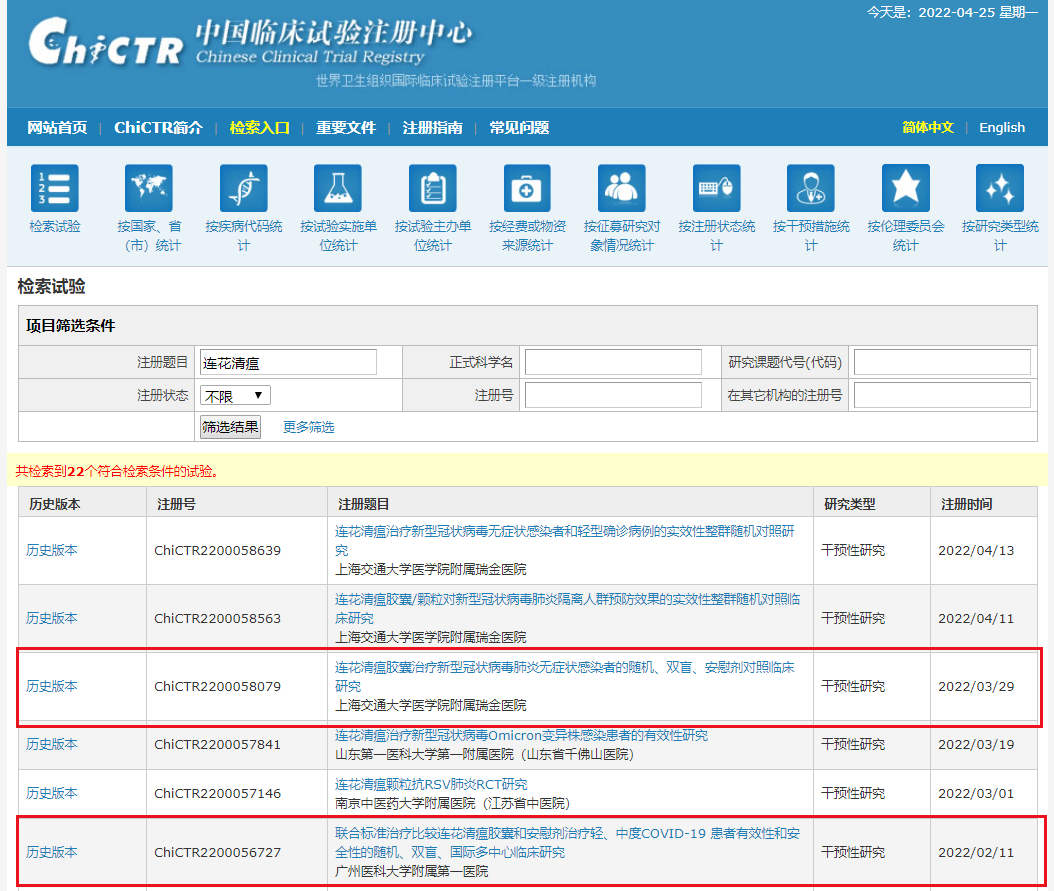
罗氏口服雌激素降解剂II期研究失败 4月25日,罗氏公布第一季度财报,同时该公司透露口服选择性雌激素受体降解剂 (SERD)giredestrant在一项治疗乳腺癌的II期acelERA试验中未能达到改善无进展生存期(PFS)的主要终点。 该项研究共招募了303例雌激素受体阳性(ER+)/人表皮生长因子受体2阴性(HER2-)局部晚期或转移性乳腺癌患者。受试者分别接受giredestrant或医生选择的阿斯利康的Faslodex(氟维司群)或芳香化酶***作为二线或三线治疗。giredestrant队列的受试者在每个为期28天的周期中每日服用一次口服SERD。 Giredestrant未能超过医生选择的内分泌单药治疗所达到的无进展生存期,导致该研究错过了主要终点。即便如此,罗氏还是从试验中得出了一些积极的结论,并指出“疗效数据令人鼓舞,对雌激素受体活性依赖程度较高的患者获益更为明显。” 该公司补充说,总生存期数据仍不成熟。 (原文有删减) 来源:医药魔方Info 国药集团中国生物奥密克戎变异株新冠灭活疫苗获NMPA临床批件 4月26日,中国生物公众号发布公告称,国药集团中国生物奥密克戎变异株(以下简称奥株)新冠**灭活疫苗获国家药监局临床批件。 国药集团中国生物在前期已上市原型株新冠灭活疫苗和完成贝塔、德尔塔变异株灭活疫苗研发的基础上,第一时间从香港大学引进奥密克戎变异毒株,2021年12月9日迅速启动了奥株灭活疫苗研发。 根据国家药监局改良型新冠疫苗指导原则和研发策略,国药集团中国生物利用新建的P3高等级生物安全实验室,完成了奥株毒种的筛选、传代、扩增,建立了三级毒种库,完成了工艺验证、多批规模化产品的制备、质量标准研究、动物体内安全性评价和免疫原性研究,结果显示奥株新冠灭活疫苗可以针对奥株及多种变异株产生高滴度中和抗体。2022年3月3日,北京生物制品研究所、武汉生物制品研究所同香港研究机构确定临床方案及相关细节,3月26日和30日分别获得中国药品食品检定研究院的检定合格报告,4月1日向香港卫生署提交了临床申请资料,4月12日获得伦理批件,4月13日获得临床研究批件,成为全球最早获批进入临床的奥密克戎株灭活疫苗。 同时,国药集团中国生物从1月26日开始向国家药监局药品审评中心*动提交国内临床申报资料,启动技术审评。 4月26日,中国生物北京生物制品研究所奥密克戎变异株新冠**灭活疫苗获得了中国国家药监局颁发的临床批件。中国生物将采用随机、双盲、队列研究的形式,在已完成2或3剂新冠疫苗接种的18岁及以上人群中进行序贯免疫临床研究,评价奥密克戎变异株新冠**灭活疫苗的安全性和免疫原性。 来源:新浪医药新闻 吉利德Veklury获美国FDA批准 近日,吉利德宣布,美国FDA已扩大了Veklury(remdesivir,瑞德西韦)的批准范围,纳入年龄在28天及以上、体重至少3公斤的COVID-19儿科患者。该批准包括因COVID-19住院的患者,以及患有轻度至中度COVID-19且有高风险进展为严重COVID-19(包括住院或死亡)的患者。 据称,Veklury是第一款也是唯一一款被批准用于治疗12岁以下COVID-19儿科患者的药物。2020年5月,Veklury获得美国FDA授予紧急使用授权(EUA),成为美国第一款治疗COVID-19的药物。同年10月,Veklury获得了FDA完全批准。 来源:一度医药 针对新冠,连花清瘟启动多项临床研究 中国临床试验注册中心官网显示,2022年共有5项连花清瘟治疗新冠肺炎的临床试验登记,包括: 联合标准治疗比较连花清瘟胶囊和安慰剂治疗轻、中度COVID-19患者有效性和安全性的随机、双盲、国际多中心临床研究; 连花清瘟治疗新型冠状**Omicron变异株感染患者的有效性研究; 连花清瘟胶囊治疗新型冠状**肺炎无症状感染者的随机、双盲、安慰剂对照临床研究; 连花清瘟胶囊/颗粒对新型冠状**肺炎隔离人群预防效果的实效性整群随机对照临床研究; 连花清瘟治疗新型冠状**无症状感染者和轻型确诊病例的实效性整群随机对照研究。 (原文有删减) 来源:医药魔方Info 由盈转亏!天士力2022年Q1净亏损5.57亿元 4月25日,天士力2022一季报显示,报告期内营业收入18.69亿元,同比增长5.97%;归属于上市公司股东的净利润为-5.57亿元,上年同期为3.2亿元,同比由盈转亏;归属于上市公司股东的扣非净利润为2.32亿元,同比减少8.79%;基本每股收益-0.3719元。 其中,中药领域表现良好,实现营业收入11.28亿元,同比增长8.45%。主要得益于公司在基层市场加大拓展力度,使复方丹参滴丸、芪参益气滴丸、养血清脑颗粒(丸)三大基药产品获得较快增长。 另外,上个月天士力发布了2021年年度报告,报告期内实现营业收入79.52亿元,同比下降41.43%,要知道,过去其曾保持了十几年10%以上的增速,高点时甚至达到65%。实现归属于上市公司股东的净利润23.59亿元,同比增长109.51%,实现归属于上市公司股东的扣非净利润为6.09亿元,同比下降26.84%,基本每股收益1.57元。 来源:新浪医药新闻 一线治疗肝癌,抗CTLA-4/PD-L1抗体组合进入优先审评 今日,阿斯利康(AstraZeneca)宣布,该公司为在研CTLA-4抗体tremelimumab递交的生物制品许可申请(BLA)被美国FDA接受并将通过优先审评渠道接受审评,与抗PD-L1抗体Imfinzi(durvalumab)联用,治疗不可切除的肝细胞癌患者。这一称为STRIDE的创新给药方案首先使用单剂tremelimumab治疗,然后患者持续接受Imfinzi治疗。阿斯利康使用了优先审评券递交这一BLA,预计在今年第四季度获得FDA的回复。 Imfinzi是一款抗PD-L1单克隆抗体,通过阻断PD-L1与PD-1和CD80蛋白的结合,解除肿瘤细胞对免疫反应的抑制。它已经在多个国家和地区获得批准治疗广泛期小细胞肺癌。并且获得FDA批准治疗非小细胞肺癌和晚期膀胱癌。 来源:药明康德 陇神戎发董事张金德、副总经理兼财务总监张帆辞职 4月25日,陇神戎发披露董事及高级管理人员辞职公告。董事会于4月23日收到公司董事张金德和副总经理兼财务总监张帆提交的书面辞职报告。 张金德因个人工作调整,不再担任公司董事,申请辞去公司第四届董事会董事职务,同时一并辞去第四届董事会薪酬与考核委员会委员职务,辞职后仍在公司工作。 张帆因个人工作变动,申请辞去公司副总经理兼财务总监职务,辞职后将不再在公司工作。 来源: 陇神戎发

最新医药动态
更多»相关资讯
更多»- 14+7完成53.2%采购量 采购总金额达11.51亿
- 2医药之梯164期|英国东南部发现新冠变种病毒、土耳其将从中国紧急采购新冠疫苗
- 3药事日报142期|我国第五款新冠疫苗进入三期临床试验将在乌兹别克斯坦开展、阿斯利康未通过COVID-19一项二期临床试验
- 4罗氏2019年业绩:国际制药业务增长11% 中国市场功不可没
- 5药事日报316期 | 多项药物临床获批,进度披露;两家药企达成研发合作协议!
- 6药事日报348期 | 千金药业外部董事接受纪律审查和监察调查!
- 7药事日报194期|礼来、GSK与Vir合作开发中和抗体组合疗法、辉瑞缩减向欧盟供应新冠疫苗
- 8药品再注册将进入新监管时代 不再“走过场”
- 9关于公布2014年浙江省药品集中采购(第一批)低价药中标产品参照价梳理结果的通知(六)
- 10恒瑞医药:中国首个醋酸阿比特龙纳米晶制剂获批上市
- 11药事日报394期 | 君实生物新冠口服药头对头临床到达主要终点!朝鲜累计发热超260万
- 12最新!16家医械巨头营收大公开 涉迈瑞、强生、美敦力
- 13国家医学中心和区域医疗中心设置实施方案发布
- 14完成成人晚发型庞贝病基因疗法临床首例受试者给药
- 15重庆市涪陵区卫生和计划生育委员会关于涪陵区基本药物采购目录内不供货的厂家及品规的通知
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
