药事日报432期 | 益方生物今日上市!募资20亿!

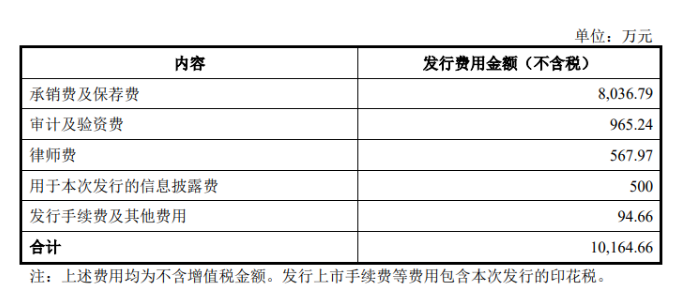
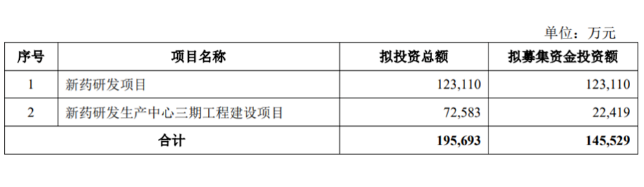
益方生物今日上市!募资20亿 益方生物科技(上海)股份有限公司(以下简称:益方生物)今日正式在科创板敲钟上市。据招股书披露,益方生物拟以18.12元/股的发行价发行11,500万股新股,其中9,949万股无流通限制及限售安排的股票于2022年7月25日起上市交易。通过本次发行,益方生物共募集20.84亿元资金,扣除1.02亿元发行成本,募集资金净额为19.82亿元。募集资金将主要用于新药研发项目和总部基地建设项目。 益方生物由王耀林(Yaolin Wang)等多位海归博士联合创办,核心产品主要聚焦于肿瘤、代谢性疾病等重大疾病领域。截至2022年6月23日,其产品管线有3个处于临床试验阶段的核心产品和5个临床前在研项目,3个核心产品均已获准开展II期或III期临床试验,研发进度均位居前列。 来源:益方生物 三星生物斥资3.23亿美元在韩国购买土地,建立第二处生产园区 7月18日,三星透露斥资3.23 亿美元在韩国仁川购买土地,用于建造新的生物制品成产园区 Bio Campus II。 三星生物旨在短期内成为合同制造龙头。因此扩张非常积极,三星生物成立仅 11 年,已有 1、2 和 3 号工厂投入运营,4 号工厂正在建设,5 号和 6 号工厂正在筹备。2018 年 3 号工厂完工时,为三星提供了单个工厂最大的 CDMO 产能,达到 360,000 升。 考虑到全球对 CDMO 服务迅速增长的需求因大流行而拖延,三星的推动时机恰到好处。去年,三星生物制品公司报告的销售额为 1.57 万亿韩元(13.1 亿美元),比 2020 年增长 35%。 来源:三星生物 14.55亿元!泽璟制药拟向特定对象发行A股募资 7月24日,泽璟制药发布公告,拟向不超过35名(含本数)符合中国证监会规定条件的证券投资 基金管理公司、证券公司、信托投资公司、财务公司、保险机构投资者、合格境外机构 投资者(QFII)、其它境内法人投资者和自然人等特定投资者发行A股募资。 公告显示,本次发行的股 票数量不超过本次发行前公司总股本的 15%,即本次发行的股票数量不超过 3,600 万股 (含本数)本次发行股票的募集资金总额不超过145,529万元(含本数),扣除发行费用后拟用于以下项目: 来源:泽璟制药 武田免疫调节新药达到3期临床主要终点 近日,武田(Takeda)宣布,其皮**射免疫球蛋白疗法HyQvia,在维持治疗慢性炎症性脱髓鞘性多发神经根***(CIDP)的随机、安慰剂对照、双盲的3期临床试验ADVANCE-1中达到其主要终点。 这项关键临床试验评估了132名成年CIDP患者使用HyQvia的疗效、安全性和耐受性。这些患者在接受治疗前至少使用了3个月稳定给药的静脉注射免疫球蛋白(IVIG)。以炎性***变原因和治疗(INCAT)残疾评分作为评判依据,主要终点分析表明,当患者以和先前接受IVIG时同样的频率和剂量进行给药时,HyQvia相比于安慰剂可显著减少CIDP的复发(9.7%对比31.4%;p=0.0045)。 来源:武田 康泰生物:上半年净利同比预降61%-70% 康泰生物公告,预计2022年半年度归属于上市公司股东的净利润1亿元-1.3亿元,同比下降61.37%-70.29%。报告期内公司业绩变动的主要原因:系新冠灭活疫苗相关资产计提减值及Ⅲ期临床支出费用化。导书等文件均为关联公司制定,企业在A区、B区的程序文件、制度文件存在两个不同版本;企业B区微生物室使用普通空调接高效过滤器的方式对空气进行净化,使用小型可移动式臭氧发生器进行室内环境消毒。 来源:康泰生物 绿叶制药醋酸戈舍瑞林缓释微球乳腺癌中国III期研究成功 7月24日,绿叶制药发布公告,称其在研新药—注射用醋酸戈舍瑞林缓释微球(LY01005)治疗乳腺癌的中国III期临床试验达到预设终点。 该III期临床为一项随机、开放、阳性药物对照的临床研究,採用非劣效试验设计,与对照药比较,评价LY01005连续肌肉注射给药治疗乳腺癌患者的有效性和安全性。 来源:绿叶制药 刚刚!阿斯利康/第一三共重磅ADC获FDA优先审评资格 今日(7月25日)消息,美国FDA已受理阿斯利康(AstraZeneca)和第一三共(Daiichi Sankyo)Enhertu治疗不可切除或转移性HER2低表达乳腺癌成人患者的补充生物制品许可申请(sBLA),并授予其优先审评资格,PDUFA预计日期在2022年第四季度。同时,该sBLA正在实时肿瘤学审评(RTOR)项目和Orbis项目下进行审评,FDA这两项举措旨在尽早为患者带来安全有效的癌症治疗。根据阿斯利康新闻稿,如果获得批准,Enhertu将重新定义转移性乳腺癌的分类和治疗,使肿瘤HER2表达水平较低的患者有机会从HER2靶向治疗中获益。 来源:药明康德 针对小核酸药物,大睿生物与赛诺菲达成合作 7月25日, 大睿生物医药科技(上海)有限公司(简称“大睿生物”)宣布与赛诺菲(Sanofi)就小核酸管线和技术平台达成独家许可交易。根据大睿生物新闻稿,该公司已经获得了赛诺菲小核酸药物平台的化学修饰和递送平台的全球独家授权,以及四个未公开靶点的临床前候选药物。此外,赛诺菲获得了在大中华地区(包括中国大陆、香港、台湾及澳门地区)以外地区大睿平台开发的针对神经和肌肉候选药物的独家购买权。根据协议条款,大睿生物将向赛诺菲支付预付款,并进一步根据研发和商业里程碑以及产品净销售额支付特许权使用费。 大睿生物成立于2021年,致力于发现和开发模块化和可编程的核酸药物,以提供给世界各地的患者。根据大睿生物官网资料,该公司已经建立了肝靶向和肝外递送平台,开发针对肝脏、中枢神经系统、眼科、肿瘤等领域的下一代高潜力产品管线。今年4月,大睿生物宣布完成3300万美元A轮融资,投资机构包括礼来亚洲基金、招银国际、Platanus、丰川投资和澜亭资本。 来源:药明康德