药事日报443期 | 辉瑞42亿美元引进的妇科口服药新适应症获FDA批准!4.15亿英镑!赛多利斯收购这家公司!

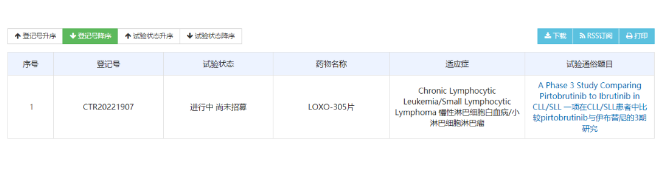
位于珠海的飞利浦健康科技新工业园区正式落成 位于珠海市金湾区三灶镇定家湾工业园内的飞利浦(珠海)健康科技新工业园区正式落成揭幕。飞利浦于1990年6月在珠海设立了子公司,经过30多年的发展,珠海园区已成为飞利浦健康生活业务全球最大的生产基地之一,服务全球,代表了飞利浦在B2C业务领域的高端制造能力和世界一流的质量运营管理。 2019年,园区决定乔迁新址,并在公司聚焦"健康科技"转型和加快在中国"本土化"进程的背景下,扩大了珠海园区的产线覆盖范围。正式揭幕的新园区,不仅生产制造男士理容、口腔健康、母婴健康等产品,还拓展到医疗领域,生产患者监护设备等医疗设备,并加大自动化和数字化的投入,旨在打造世界级的先进制造运营中心,立足中国,服务全球。 来源:美通社 4.15亿英镑!赛多利斯收购重组白蛋白公司Albumedix 8月8日,德国生命科学集团赛多利斯(Sartorius)宣布通过其在法国上市的子公司Sartorius Stedim Biotech同意从私人投资者手中收购Albumedix Ltd.公司100%的股份。 Albumedix总部位于英国诺丁汉,被公认为重组人白蛋白产品和技术的全球领导者。 此次收购价格约为4.15亿英镑。该交易有待监管部门批准,预计将于2022年第三季度末前完成。 来源:医药魔方 清华孵化,清大高端完成千万级Pre-A轮融资 近日,清大高端正式宣布完成千万级人民币Pre-A轮战略融资,本轮融资由九强生物董事长邹左军领投,募集资金主要用于清大优氧微粒径负氧离子项目的技术研发和产品升级。疫情常态化让国人对呼吸健康有了更多关注,此轮融资将进一步推进清大高端在原有技术优势上进行产业结构调整,多层次、全方位立体化推动人居环境空气优化,践行“让国人呼吸更健康的空气”企业使命。 清大高端公司是为清华大学天津高端装备研究院孵化企业,由江西省**以招商引资形式进驻九江市,清大高端深耕人工生成负氧离子技术,是国内首个人工生成负氧离子技术行业团体标准的起草制定单位。本次募集资金具体包括对该项目的技术研发投入,提升产能和工艺稳定性,加强品牌市场推广端投入以及高端人才引进,进一步巩固清大高端在人工生成负氧离子领域的竞争优势。 来源:医药魔方 礼来BTK***在中国启动3期临床研究 8月8日,中国药物临床试验登记与信息公示平台显示,礼来公司(Eli Lilly and Company)登记了一项LOXO-305片治疗慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)的国际多中心(含中国)3期临床试验。 公开资料显示,pirtobrutinib(即LOXO-305)是一款口服、高选择性、非共价(可逆的)BTK***,正在进行多项全球3期临床研究。就在近日,该药还获得美国FDA授予的优先审评资格,用于治疗经治套细胞淋巴瘤患者。今年3月,礼来与信达生物达成产品授权合作,授予信达生物享有pirtobrutinib未来在中国大陆商业化权利的优先谈判权。 来源:医药观澜 2.34亿美元!翰森制药与Tiumbio合作开发GnRH拮抗剂 8月8日,翰森制药公告宣布,其全资附属公司翰森(上海)健康科技有限公司及江苏豪森药业集团有限公司(统称为被许可人)与TiumBio订立独家许可协议。 根据许可协议,被许可人获得TiumBio的独家许可,以于中国(包括香港、澳门及台湾)开发及商业化TU2670用于**内膜异位症和**肌瘤及其他潜在适应症的治疗。被许可人将负责TU2670于中国的开发、注册审批及商业化,并将支付450万美元首付款,150万美元的技术转让费及最多1.64亿美元的开发、注册及基于销售的商业化里程碑潜在付款,以及基于产品净销售额的分级特许权使用费。 TiumBio总部位于韩国,是一家以研发为重点的生物制药公司,致力于发现和开发创新的小分子和生物药物。该公司目前正在开发免疫肿瘤学、纤维化、**内膜异位症/**肌瘤和血友病等领域的临床和临床前候选药物。 来源:医药魔方 辉瑞42亿美元引进的妇科口服药新适应症获FDA批准 近日,辉瑞/Myovant Sciences宣布,FDA已批准Myfembree(40mg relugolix+1mg 雌二醇+0.5mg 醋酸炔诺酮)用于治疗绝经前妇女**内膜异位症相关的中度至重度疼痛,每日一次,每次一片,疗程最长24个月。此前,Myfembree已被FDA批准用于治疗**肌瘤相关**大量出血。 2020年12月,辉瑞与Myovant Sciences达成协议,在美国和加拿大合作开发和商业化肿瘤学和妇女健康领域新药relugolix及其复方片剂,交易总额高达42亿美元。 来源:辉瑞/Myovant Sciences 国内首个!甘李药业每周1次胰岛素制剂获FDA批准开展I期临床试验 8月8日,甘李药业公告宣布,其自主研发的超长效胰岛素周制剂GZR4获FDA批准开展I期临床试验,试验由其全资子公司甘李药业(美国)负责。 目前已上市的长效基础胰岛素类似物主要有甘精胰岛素、地特胰岛素和德谷胰岛素。据公开财报显示,2021年上半年甘精胰岛素(来得时)、地特胰岛素(诺和平)和德谷胰岛素(诺和达)的全球销售额分别为25.42亿、7.78亿、13.33亿美元。 截至2022年3月31日,甘李药业在GZR4项目中累计投入研发费用4617万元人民币。此次GZR4在美国临床获批,有望进一步为全球糖尿病患者带来革新性的治疗选择。 来源:甘李药业 最新!中国发现新**,人畜共患,已感染35人 根据澎湃新闻报道,日前在《新英格兰医学》杂志上,中国、新加坡两国的科学家日前联合发表通讯文章,称中国山东、河南两地发现一种可感染人类的动物源性亨尼帕**。 这篇文章是中国军事科学院军事医学研究院微生物流行病研究所的刘玮、方立群、杜克-新加坡国立大学医学院王林发三位教授及其他学者共同完成的。 据悉,亨尼帕**是亚太地区人畜共患病的重要新兴病因之一,目前已知会感染人类并导致致命疾病,被列为生物安全四级**,致死率在40%至75%之间,远远高于新冠**。感染这种**的症状有发热、乏力、咳嗽、厌食、肌痛、恶心等。 科学家通过研究,在一名患者的咽拭子样本中发现了一种新型的亨尼帕**,并命名为“琅琊**”。琅琊**由18402个核苷酸组成,基因组组织与其他亨尼帕**相同;进化关系上,其与之前在云南墨江发现的亨尼帕**最相关。 进一步调查发现,中国山东、河南两地已有35例“琅琊**”感染者,其中26例出现了发热、发力、咳嗽、厌食、肌痛、恶心、头痛、呕吐等临床症状。 对于亨尼帕**,目前尚无有效的疫苗和药品。 来源:江淮医学