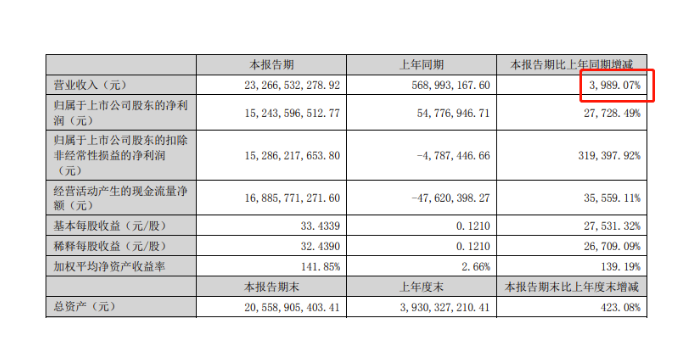
药事日报457期 | 净利润152亿!九安医疗发布半年报

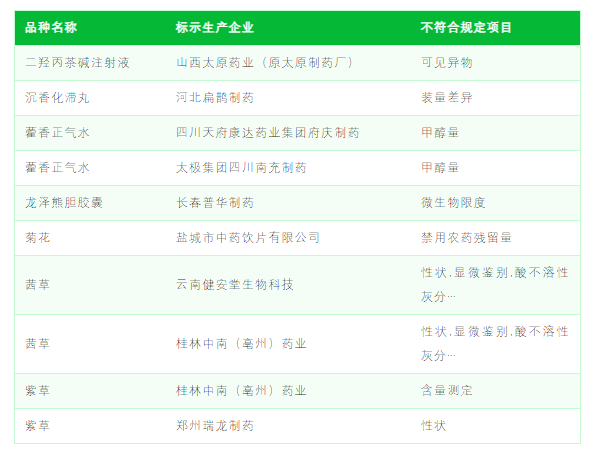
国产首款!通化东宝「德谷胰岛素利拉鲁肽注射液」申报临床 8月29日,CDE网站显示,通化东宝的德谷胰岛素利拉鲁肽注射液的临床试验申请已获受理。 该复方制剂最早由诺和诺德开发,于2014年9月首次获批上市,商品名为Xultophy,适应症为2型糖尿病。它也是全球首款长效胰岛素/GLP-1复方制剂。 德谷胰岛素(insulin degludec)是一种超长效基础胰岛素类似物,具有半衰期长、作用平稳持久、低血糖发生风险更低的特点。由诺和诺德公司开发,2012年10月首次在日本获批上市,商品名为Tresiba,随后分别于2015年和2017年在美国和中国获批上市。 来源:CDE网站 班科生物完成超千万元天使轮融资,加速新型抗**纳米抗体药物研发 近日,从事新型纳米抗体药物研发企业武汉班科生物技术有限公司(以下简称“班科生物”)完成超千万元天使轮融资,本轮融资由武汉东湖高新股权投资管理有限公司(以下简称“东湖投资”)领投,共同参与投资的还有武汉生物技术研究院下属武汉百赢生物产业投资管理有限公司(以下简称“百赢投资”)。 本轮融资将用于班科生物抗**纳米抗体药的临床前研究,以及其他研发管线的推进和团队建设。 来源:医药魔方 桃子健康完成数千万元C轮融资,和达资本已连投三轮 近日,四川桃子健康互联网医院管理有限公司(以下简称:桃子健康)完成数千万元C轮融资,本轮由和达资本领投。和达资本以对桃子健康连投三轮的持续关注,既是其对桃子健康的深度认可和持续支持,也展现出对数字医疗赛道未来发展的坚定看好。 桃子健康成立于2017年,是一家数字医疗产业的综合服务商。公司抢抓数字医疗产业发展机遇,结合产业发展的综合需要,提出两平台六中心的模式,帮助产业链上的企业提供从建设到运营的全生命周期协同服务。 桃子健康旗下全资和控股企业包括成都华府医院、桃子互联网医院、海豚怡新、九兴医药、康仁百草堂等9家医疗、医药公司。桃子健康于2018年获得行业主管部门颁发的互联网医院牌照,成为成都市首家互联网医院。集团旗下的互联网医院以数字技术赋能基层医生,面向互联网医疗、数字医药产业提供全科在线问诊服务。集团连续三年入选未来医疗100强。 来源:桃子健康 全球罕见!江苏发现2例黄金血型 近日,南京医科大学附属泰州人民医院接诊了一名重度贫血女子,该女子血型全球罕见,全球不足50例。该院输液科主任高灵宝介绍,通过调查发现患者亲姐姐的血型也和其一样。 该院输血科在对王女士进行血型和血型抗体检查时发现,她不仅仅是RhD阴性(俗称熊猫血),而且其RhC、Rhc、RhE、Rhe均为阴性(RhNULL),再加上其ABO血型为O型,红细胞上再也没有任何血型抗原。 这就意味着如果她作为献血者的话,可以将自己的血提供给任何一个需要输血的病人,而不管这个受血者是啥血型。很遗憾的是,这种血型的人一旦生病需要输血,往往只能接受与其同样血型的血液。 来源:快科技 缓解率显著提升!达雷妥尤单抗+RVd一线治疗多发性骨髓瘤II期结果积极 8月27日,强生旗下杨森公布了一项关键II期GRIFFIN研究的最终分析结果。该研究旨在评估Darzalex(达雷妥尤单抗)四联疗法治疗符合自体干细胞移植(ASCT)条件的新诊断多发性骨髓瘤成年患者的疗效。 达雷妥尤单抗是全球首个获批用于治疗多发性骨髓瘤的靶向CD38的全人源单克隆抗体,可直接与骨髓瘤细胞表面重要的免疫治疗靶点CD38特异性结合,通过多重机制诱导骨髓瘤细胞死亡,达到快速缓解的治疗效果。2012年8月,强生和Genmab达成一项全球协议,授予杨森开发、生产和商业化达雷妥尤单抗的独家授权。 来源:医药魔方 净利润152亿!九安医疗发布半年报 2022年8月29日,九安医疗(002432)披露半年度报告,公司2022年半年度实现营业收入为232.67亿元,同比增长3989.07%;归母净利润152.44亿元,同比增长27728.49%;基本每股收益33.43元。 报告期内,九安医疗将主要精力和资源投入到iHealth试剂盒产品的研发、生产和销售中,由于iHealth试剂盒产品在报告期内销售收入大幅增长,公司本报告期业绩较去年同期也出现大幅上升。iHealth系列产品营业收入较去年同期增长7480.04%,毛利率达到81.66%,对本报告期业绩的大幅上升做出了重要贡献。 来源:九安医疗 再生元:NASH新药HSD17B13 siRNA启动二期临床 2022年8月29日,再生元在Clinicaltrials.gov网站上注册了ALN-HSD的二期临床试验。 ALN-HSD为靶向HSD17B13的siRNA疗法,为再生元基因药物中心(RGC)的首发管线。该二期临床计划入组300例NASH患者。 来源:翰森制药 9家药企被通报,暂停销售,立案调查! 今日,国家药监局发布通告,经中国食品药品检定研究院等 6 家药品检验机构检验,标示为郑州瑞龙制药股份有限公司等 9 家企业生产的紫草等 20 批次药品不符合规定。 《通告》中,对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。 国家药品监督管理局要求相关省级药品监督管理部门依据《****共和国药品管理法》,组织对上述企业和单位存在的涉嫌违法行为立案调查,并按规定公开查处结果。 来源:国家药监局