药事日报463期 | 辉瑞116亿美元收购获得的偏头痛药物在华申报上市
时间:2022/09/07来源:医药之梯阅读:335

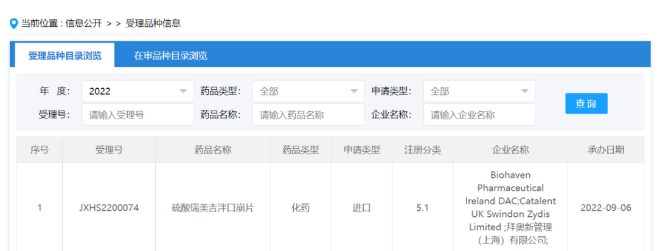
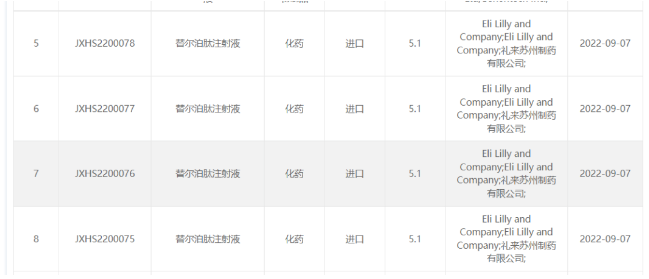
博士伦干眼病新药向FDA申报上市,恒瑞拥有中国权益 9月6日,Bausch+Lomb(博士伦)和Novaliq共同宣布,FDA已受理其NOV03滴眼液用于治疗睑板腺功能障碍(MGD)相关干眼病的上市申请,并将PDUFA日期定为2023年6月28日。 2019年11月,恒瑞与Novaliq达成合作,获得NOV03滴眼液和CyclASol(0.1%环孢素A制剂)在中国的独家临床开发、生产和商业化权。同年12月,Bausch Health与Novaliq达成合作,获得NOV03滴眼液在美国和加拿大的独家开发和商业化权。目前,恒瑞已成功完成NOV03滴眼液(SHR8058)在国内的III期临床试验。 来源:医药魔方 利那洛肽治疗儿童功能性便秘III期成功,拟申报上市 9月6日,Ironwood公告宣布,其鸟苷酸环化酶C激动剂利那洛肽一项III期研究成功,治疗儿童功能性便秘(FC)患者。这是首款在III期研究中证明对儿童FC患者有效的药物。Ironwood表示,将与艾伯维共同推进该适应症的上市申请。 便秘是一种儿童时期常见的胃肠道疾病,其中FC约占儿童便秘的90%~95%,其临床表现为排便次数减少、排便不尽感和持续性排便困难。 来源:Ironwood 主攻“不可成药”靶点!罗氏达成合作 9月6日,PhoreMost 宣布已与罗氏达成了多项关于靶点发现的相关合作。根据协议,PhoreMost将获得预付款,并有资格获得基于临床前成功的里程碑付款。2020年,PhoreMost与勃林格殷格翰也达成了多项合作。 利用SITESEEKER平台,PhoreMost将针对罗氏选定的血液学和免疫学疾病相关通路进行筛选,确定的新靶点交由罗氏的研发部进一步验证与表征。 来源:医药魔方 2.2亿美元助力制造可编程CAR-T疗法,新锐剑指实体瘤 今日,Arsenal Biosciences公司宣布完成2.2亿美元的B轮融资。获得资金将用于扩展其可编程细胞疗法研究活动,增长其用于治疗多种实体瘤的候选疗法管线。该公司正在为主打疗法AB-105准备临床试验。这一用于治疗*巢癌的疗法的IND申请已经获得美国FDA的许可,预计今年晚些时候完成首例患者给药。 CAR-T疗法在治疗血液癌症方面已经获得了出色的疗效,然而在治疗实体瘤方面仍然面临着多重挑战。ArsenalBio公司的策略结合CRISPR基因编辑,合成生物学和逻辑门控回路,对CAR-T细胞进行重新编程。新闻稿指出,该公司正在构建行业中最大型的治疗增强整合回路文库,利用逻辑门控改善肿瘤靶向,并且通过合成生物学让CAR-T疗法具有行使多种药物功能的潜力。 来源:药明康德 辉瑞116亿美元收购获得的偏头痛药物在华申报上市 9月6日,CDE官网显示,Biohaven公司的偏头痛药物硫酸瑞美吉泮口崩片(Rimegepant)上市申请获国家药监局受理,推测该适应症为:用于成人急性偏头痛的治疗。 Rimegepant是一款口服CGRP受体拮抗剂,于2020年2月首次获FDA批准用于成人急性偏头痛的治疗,2021年5月,又扩展新适应症,用于预防成人发作性偏头痛。 来源:CDE官网 辉瑞多位高管迎来新任命 近日,辉瑞多位高管迎来了新任命,涉及肿瘤、罕见病和商业战略创新部门负责人。辉瑞表示,此次高管变动是出于商业战略的考虑,同时也为员工提供成长和发展的机会。 现肿瘤全球总裁Andy Schmeltz被任命为公司商业战略和创新高级副总裁,负责投资组合战略和投资决策。他已在辉瑞工作了19年,4年前开始担任肿瘤全球总裁。 现罕见病部门负责人Suneet Varma接任肿瘤全球总裁。Suneet Varma已在辉瑞工作了21年,曾担任过消费者保健和医院等多个部门负的责人。而罕见病部门将由现全球专科护理总裁Kevin Sullivan领导。 来源:辉瑞 礼来GIP/GLP-1双激动剂tirzepatide在国内申报上市 9月7日,CDE官网显示,礼来的葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂Mounjaro(tirzepatide)上市申请获受理,用以改善成人2型糖尿病患者的血糖控制。Mounjaro是近10年来,首个新糖尿病药物类型。 此外,Tirzepatide在减重方面也取得了成功,在III期SURMOUNT-1试验中,tirzepatide (5mg, 10mg, 15mg) 治疗组患者第72周时的减重效果均显著优于安慰剂对照组,平均减重最高达到22.5% (24kg),而且15mg高剂量组有63%的患者减重达到20%以上。礼来表示将与FDA讨论并寻求这一适应症的监管批准 来源:医药魔方 欧盟否决71亿美元收购合并 Illumina或将剥离Grail 据华尔街日报报道,美国生命科学公司因美纳(Illumina)将不得不剥离生物技术公司Grail,此前欧盟否决双方71亿美元合并,担心会损害竞争并扼杀创新。 欧盟委员会竞争事务专员维斯塔格表示,调查表明因美纳在下一代测序方面占据主导地位,将有能力和动机阻挠竞争对手。在这个关键的发展阶段,保持早期癌症检测开发商之间的竞争至关重要。去年8月,因美纳在欧盟监管部门批准之前完成交易,结果欧盟命令Grail保持独立,并任命独立经理人管理该公司,直到调查结束。 来源:华尔街日报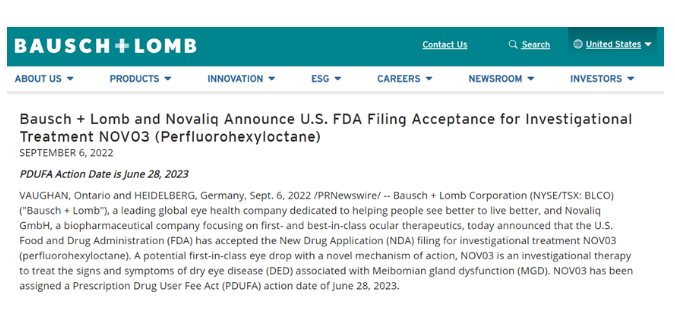



最新医药动态
更多»相关资讯
更多»- 1艾伯维JAK抑制剂第2项特应性皮炎III期试验成功
- 2药事日报532期 | 复必泰mRNA疫苗于中国香港获批上市!
- 3药品院外市场观察:诺华、拜耳等老牌MNC密集牵手互联网
- 4药事日报242期 | 强生(JNJ.US)宣布将取消在印度本地的新冠疫苗试验 湘泉药业董事邓淞元辞职
- 5德琪医药C轮融资9700万美元,主要用于新药研发和商业化
- 6关于妇儿、急(抢)救目录药品挂网交易相关情况的通知
- 7药事日报143期|moderna新冠肺炎疫苗近95%有效、钟南山称中国疫苗保护水平与辉瑞疫苗不相上下
- 8最新数据惊艳亮相!ESMO重磅:这款“革命性”抗癌药带来两大惊喜!
- 9罗氏2019年业绩:国际制药业务增长11% 中国市场功不可没
- 10关于公布吉林省医疗机构基础输液和常用低价药品直接挂网第二批审核结果的通知
- 11药事日报491期 | 罗氏近10亿美元引进病毒免疫疗法!艾伯维2.55亿美元现金收购DJS!
- 12《赣州医疗机构“不满意就退费”工作实施方案(试行)》征求意见稿在网上引热议
- 132015年度贵州省药品集中采购公告(二)
- 14关于暂停上海庆安药业集团宿州制药有限公司珍黄胶囊的通知
- 15药企缺乏人才领袖?技能短缺成为生命科学创新迫在眉睫的威胁
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
