11.88亿美元 乐普生物就CMG901与AstraZeneca订立独家许可协议
2月23日,乐普生物发布公告,公司与康诺亚成立的合营企业KYM Biosciences Inc.与AstraZeneca AB(一家全球制药公司)订立全球独家许可协议,协议约定将Claudin18.2 ADC新药CMG901的全球权益授权给AstraZeneca AB,后者支付6300万美元预付款、11.25亿美元里程碑金额以及一定比例的销售分成。

据公开资料显示,CMG901由乐普生物和康诺亚共同开发,乐普生物负责ADC技术,康诺亚负责抗体。是靶向Claudin 18.2的抗体偶联药物(ADC),含Claudin 18.2特异性抗体、可裂解连接符及毒性载荷、一甲基澳瑞他汀E(MMAE)。其为首个在中国及美国均取得临床试验申请许可(IND)的Claudin 18.2抗体偶联药物。Claudin 18.2于胃癌、胰腺癌及其他实体瘤中的表达呈高度选择性及广泛性,使其成为癌症治疗的理想靶点。乐普生物负责ADC技术,康诺亚负责抗体。
1月28日,康诺亚在2023 ASCO GI会议上报告了CMG901的初步临床数据截至2022年8月4日,CMG901 Ia期临床研究共入组27例患者(13例患有胃癌/胃食管结合部腺癌,14例患有胰腺癌)。研究结果显示,CMG901安全性和耐受性良好,3/27例(11.1%)患者发生药物3级相关不良事件,没有发生4级及以上药物相关不良事件。剂量递增成功至3.4 mg/kg,且尚未达到最大耐受剂量(MTD)。仅2.2 mg/kg组1例患者发生剂量限制性毒性。
疗效方面,8例接受CMG901治疗的Claudin 18.2阳性胃癌或胃食管结合部腺癌患者中,客观缓解率为75%,疾病控制率为100%。其中,2.6、3.0和3.4mg/kg队列患者的客观缓解率均为100%。中位无进展生存时间(mPFS)和中位总生存时间(mOS)均尚未达到。
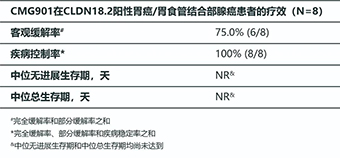
图片来源: 康诺亚公众号
反观AstraZeneca 作为全球领先的制药公司, 在ADC领域布局已久,尤其是与第一三共合作的DS-8201,仅2022年上半年销售额就达到2.05亿美元,相较于2021年同期增长了超过2倍,并且仍处于高速增长阶段。此次引进乐普生物的Claudin18.2 ADC,表明其对CMG901的高度认可。