药事日报387期 | 默沙东抗病毒新药在中国获批上市!北京封城静默系谣言!

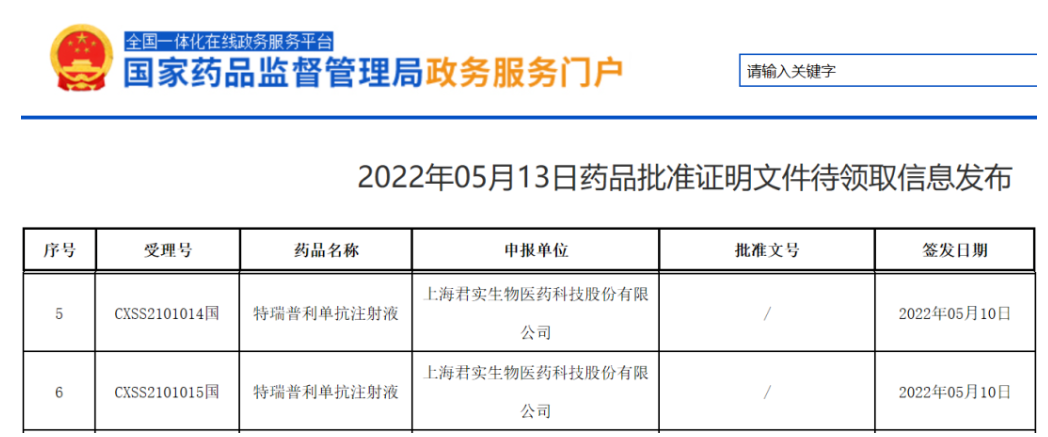
四环医药称私有化等新闻内容不属实,涨幅收窄 5月12日,有消息称华润就将四环医药私有化事宜进行磋商。 对此,据彭博社报道,针对网传华润集团正与四环医药私有化进行谈判,以及相关估值、私有化作价等信息,四环医药表示:“私有化等新闻内容不属实,四环医药并未与华润集团或其他任何机构或组织商讨上述事项,亦没有计划将本集团私有化。” 此前,四环医药一度因传闻拉升涨超24%,目前涨幅收窄至5%以内。 来源:四环医药 Caribou即用型CAR-T疗法达到100%总缓解率 今日,Caribou Biosciences公司宣布,其基于CRISPR基因编辑改造的即用型CAR-T疗法CB-010,在治疗复发/难治性B细胞非霍奇金淋巴瘤患者的1期临床试验中获得积极结果。在接受初始剂量的5名患者中,获得100%总缓解率和80%的完全缓解率。新闻稿指出,CB-010是首款获得100%总缓解率的同种异体CAR-T疗法,也是首款携带PD-1敲除的临床期同种异体CAR-T疗法。 Caribou Biosciences由诺奖得主,CRISPR领域先驱Jennifer Doudna博士联合创建,致力于利用CRISPR基因编辑技术,开发变革性疗法。该公司的主打CAR-T疗法CB-010利用基因编辑技术生成,除了表达靶向CD19的嵌合抗原受体(CAR),还利用基因编辑敲除了免疫检查点蛋白PD-1的表达,旨在提高抗肿瘤活性的持久性。 来源:药明康德 北京:封城静默系谣言,外卖快递配送不停 5 月 12 日北京疫情发布会报告,12 日 0 时至 15 时北京新增本土新冠病例 28 例。目前两条独立传播链条基本清晰,但社会面仍存在隐匿传染源,疫情传播尚未完全阻断。 发言人徐和建提示,所谓封城静默都是谣言,抢菜囤购等没必要。北京民生保障物资货源充足,外卖快递配送不停,请市民理性购物,不需要紧张。 来源:央视新闻 国家卫健委人口文化发展中心原主任涉嫌严重违纪违法 据**纪委国家监委驻国家卫健委纪检组,国家卫健委人口文化发展中心原主任奉雯涉嫌严重违纪违法。 目前正接受**纪委纪律**和河北省保定市监委监察调查。 来源:**纪委国家监委网站 NIH与MPP、WHO达成许可协议,允许各国药企使用 5月12日,世界卫生组织(WHO)宣布,其新冠肺炎技术获取池(C-TAP)联合药品专利池(MPP)与美国国立卫生研究院(NIH)达成了一项许可协议。NIH将11项新冠肺炎专利技术授予给前者,以便让更多企业获得这些技术,开发更多满足当前和未来公共卫生需求的商业产品。 这些许可是透明的、全球性的和非排他性的,允许世界各地的药企与MPP、C-TAP合作,使中低收入国家的人们可以获得这些技术,帮助结束新冠疫情。在大多数情况下,NIH不会对被***列为最不发达的49个国家的许可产品收取版税。。 协议中的11项新冠肺炎专利技术包括疫苗开发使用的融合前刺突蛋白、以及其它开发、研究、诊断工具。 来源:医药魔方 君实生物PD-1特瑞普利单抗在华获批第5项适应症 5月13日,NMPA官网最新公示,君实生物研发的PD-1***特瑞普利单抗(拓益)新适应症上市申请已获批。根据公开资料,此次获批适应症为联合含铂化疗一线治疗局部晚期或转移性食管鳞癌,这也是特瑞普利单抗在中国获批的第5项适应症。 特瑞普利单抗是君实生物自主研发的重组人源化抗PD-1单克隆抗体注射液,此前已在中国获批4项适应症,包括:1)用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗;2)用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗;3)用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗;4)联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗。 来源:NMPA官网 默沙东抗**新药「来特莫韦注射液」在中国获批上市 今日,中国国家药监局(NMPA)官网最新公示,默沙东(MSD)抗**新药来特莫韦(letermovir)注射液剂型已获批上市。值得一提的是,该药的片剂剂型已经于今年1月在中国获批,用于巨细胞**的预防性治疗。 巨细胞**(CMV)作为一种广泛存在的疱疹**,对造血干细胞移植(HSCT)患者的生命健康构成了严重威胁。研究表明,这些患者当中,巨细胞**的血清阳性率可高达92%,**复燃比例高达30~80%。根据默沙东早先新闻稿介绍,在来特莫韦问世前,全球尚无批准用于异基因HSCT后预防CMV感染的药物。虽然抢先治疗是控制CMV的有效方法,但仍有很多异基因HSCT受者会出现难治性巨细胞**感染问题,且抢先治疗药物存在骨髓抑制、肾毒性等不良反应问题,增加了患者的死亡风险和医疗负担。 来特莫韦是一种新型非核苷CMV***(3,4-二氢喹唑啉)。公开资料显示,该产品具有新型抗CMV的作用,通过抑制巨细胞**末端酶复合物的活性,阻止**DNA的加工和包装,从而发挥抗**的作用。与DNA聚合酶***的不同之处在于,来特莫韦对CMV选择性更高,作用强度也有明显提高。 来源:NMPA官网