海思科创新抗肿瘤小分子药物IND申请获受理
12月11日,海思科医药集团股份有限公司发布公告称其全资孙公司西藏海思科制药有限公司收到国家药品监督管理局下发的《受理通知书》,基本情况如下:


HSK39775是公司自主研发的一个全新的具有独立知识产权的治疗晚期实体瘤的药物,有潜力用于治疗同源重组修复缺失相关癌症,尤其是与BRCA突变相关的癌症,如乳腺癌、*巢癌及前列腺癌。根据国家药品监督管理局关于发布《化学药品注册分类及申报资料要求》的通告(2020年第44号)中化学药品注册分类的规定,本品属于化学药品1类。
临床前研究结果显示,HSK39775在多个肿瘤细胞系中显示出潜在疗效,并在同源重组修复缺陷模型中具有强效的抗肿瘤活性。此外,HSK39775在临床前安全性实验中表现出良好的耐受性和较大的安全窗,是一款极具开发潜力的小分子药物。目前,全球同靶点药物大多处于早期研发阶段,其中最高研发阶段为I期临床。
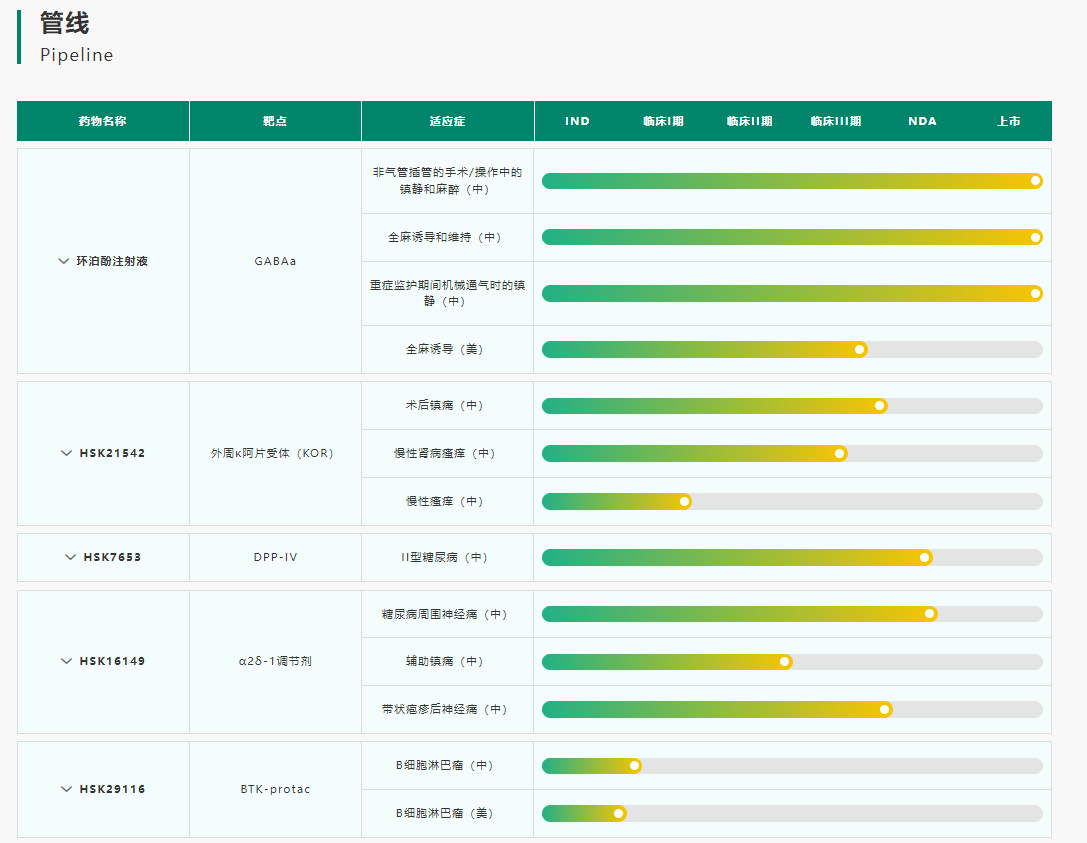
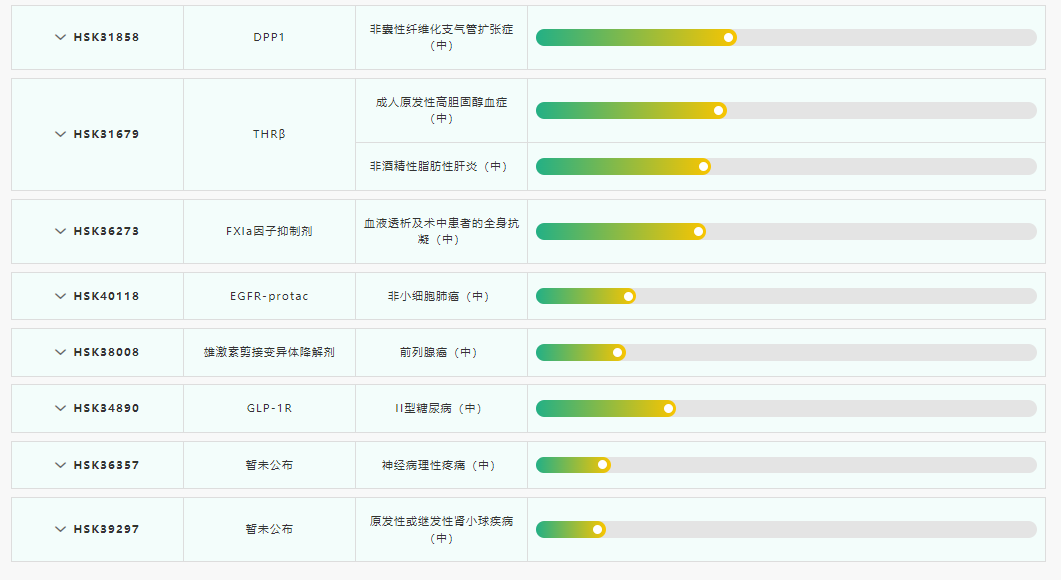
IND申报方面,2023年至今海思科已有9款1类新药提交临床申请,其中7款1类新药HSK40118片、HSK37251片、HSK38008干混悬剂、HSK31679片、HSK34890片、HSK21542片、HSK36357胶囊已相继获批临床,进一步丰富公司创新研发管线。