药事日报511期 | 60亿元!复星医药引进复宏汉霖「斯鲁利单抗」商业化权益!
时间:2022/11/18来源:医药之梯阅读:290

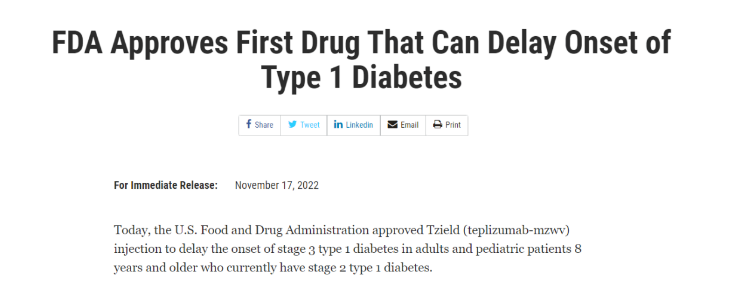
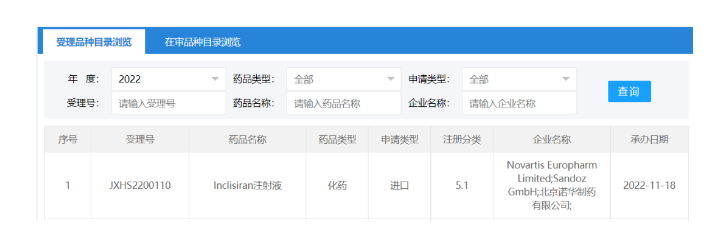
60亿元!复星医药引进复宏汉霖「斯鲁利单抗」商业化权益 11月17日,复宏汉霖发布公告,称已与复星医药子公司复星医药产业订立许可协议,同意基于本公司知识产权授予后者于区域内及领域内商业化汉斯状(斯鲁利单抗注射液)的独家许可。 根据协议条款,复宏汉霖将基于公司知识产权授予复星医药一项独家许可(附有分许可权利,惟未经本公司事先书面同意(但复星医药产业分许可给FosunPharma,或在分许可后仍保持主要负责和控制许可产品在区域内及领域内的商业化的情况除外),复星医药不得将其主要商业化权利授出分许可或转让予任何第三方),供其于区域内及领域内商业化许可产品。 复星医药须向复宏汉霖支付首付款10亿元人民币,一次性监**程碑款项5000万美元(约合3.58亿元人民币),最多6.5亿美元(约合46.52亿元人民币)销售里程碑付款,以及特许权使用费等。 来源:复宏汉霖 超20亿美元!再生元与CytomX合作开发新一代双抗 11月17日,再生元与CytomX Therapeutics宣布达成一项合作和许可协议,利用CytomX的Probody therapeutic平台以及再生元的Veloci-Bi双特异性抗体开发平台,开发条件性激活的试验性新一代双特异性癌症疗法。 根据协议条款,再生元和CytomX将合作开展临床前发现研究,以确定和验证具有条件活性的双抗。再生元将负责资助临床前和临床开发和商业化活动。CytomX将获得3000万美元的预付款,未来的靶标提名付款,最多20亿美元的研究、开发、监管和销售里程碑付款,以及特许权使用费。 CytomX是首家提出ProBody技术的企业,并凭借该技术入选了2013年Fierce 15 Biotech公司名单,随后就该技术与安斯泰来、BMS和Immunogen达成合作,产品管线如下。 来源:医药魔方 百济神州「泽布替尼」获欧盟批准治疗慢性淋巴细胞白血病 11月17日,百济神州宣布,欧盟委员会(EC)已批准百悦泽(泽布替尼)用于治疗初治(TN)或复发/难治性(R/R)慢性淋巴细胞白血病(CLL)成人患者。这是该BTK***在欧盟获批的第2项适应症。 本次EC的批准基于两项3期临床试验的积极结果。这两项试验为在既往未经治疗的CLL患者中开展的SEQUOIA试验(NCT03336333)和在R/R CLL患者中开展的ALPINE试验(NCT03734016)。 来源:百济神州 全球首款延缓或预防1型糖尿病疗法获批 11月17日,FDA官网显示,Provention Bio的CD3单克隆抗体Teplizumab已获FDA批准上市,用于延缓或预防成人及8岁以上人群的临床1型糖尿病,成为了全球首款改变1型糖尿病疾病进程的疗法。 1型糖尿病(T1D)是一种自身免疫性疾病,其发病机制为免疫系统错误地攻击胰岛β细胞,导致胰岛素缺乏,机体无法维持正常的血糖水平。近一个世纪以来,胰岛素替代疗法是大多数患者的唯一治疗方法。 Teplizumab是一款靶向T细胞表面CD3抗原的单抗,通过与效应T细胞表面的CD3结合,抑制T细胞对胰岛β细胞的攻击,从而保护胰岛β细胞不受**。Teplizumab的Fc段经氨基酸修饰后,构成了Fc受体非结合(FNB)区域,减少与补体和Fc受体的结合并降低了相关毒性反应。 来源:医药魔方 正式纳入突破性治疗品种!荣昌生物泰它西普再获重磅认定,针对重症肌无力 11月17日,荣昌生物制药(烟台)股份有限公司(688331.SH/09995.HK)宣布,注射用泰它西普(研发代号:RC18;商品名:泰爱)正式被国家药监局药品审评中心(CDE)纳入突破性治疗品种,用于治疗全身型重症肌无力。 突破性治疗药物是指用于防治严重危及生命或者严重影响生存质量的疾病,而且尚无有效防治手段,或与现有治疗手段相比具有更显著或者更重要的创新药或改良型药物。对纳入突破性治疗药物的创新药,国家药监局药审中心将优先配置资源进行沟通交流,新药上市时间将大大缩短。 来源:荣昌生物 首款!糖尿病新药刚刚获批,有效延缓糖尿病发作 今日,美国FDA宣布已经批准Provention Bio公司的药物Tzield(teplizumab)上市,用于延缓1型糖尿病特定高危人群的疾病进程。美国FDA的新闻稿指出,这也是首款能延缓1型糖尿病发作的药物。 1型糖尿病是一种慢性疾病。由于患者的胰腺β细胞受损,他们体内分泌的胰岛素量非常少,甚至可以几乎为零!胰岛素是身体的一种重要激素,分泌不足会导致血糖水平的异常升高和糖代谢异常,诱发一系列代谢问题。 多种因素都可能导致1型糖尿病的发生。尽管科学界针对这一疾病已开展了大量的研究,目前我们仍然没有彻底治愈该疾病的方法。而在胰岛β细胞被彻底损坏之前进行干预,对于保存β细胞功能、缓解病情进展有着重要意义。 来源:药明康德 维昇药业在港交所递交IPO申请 11月17日,香港证券交易所公示显示,维昇药业已向港交所递交IPO申请,并获得受理。维昇药业成立于2018年11月,专注于为大中华区大量医疗需求未被满足的特定内分泌疾病患者提供创新治疗方案。自成立以来,维昇药业已建立包含3款候选药物的产品管线。其中,核心产品隆培促生长素已在中国3期临床中达到主要终点,预计2023年向中国国家药监局(NMPA)递交上市申请。 来源:维昇药业 每年只需注射2次!诺华全球首创siRNA降血脂新药在华申报上市 11月18日,诺华在中国提交的Inclisiran注射液上市申请获得CDE受理。该药是诺华97亿美元收购The Medicines Company获得的一款首创小分子干扰RNA(siRNA)降胆固醇药物,每年只需两次皮下给药。 Inclisiran是一款first-in-class siRNA药物,能够与RNA诱导沉默复合体(RISC)结合,并在反义链的介导下与编码PCSK9蛋白的mRNA结合,抑制PCSK9蛋白的产生。从而阻止PCSK9介导的与低密度脂蛋白受体(LDLR)降解,使得能够清除血液中低密度脂蛋白的LDLR的数量增加,从而降低LDL-C水平。 来源:诺华





最新医药动态
更多»相关资讯
更多»- 1构成人体病毒组的病毒多达380万亿多个
- 2阿斯利康创新酶替代疗法在中国获批临床
- 3一线治疗胃癌!奥赛康药业抗CLDN18.2单抗启动关键3期临床
- 4赛诺菲:重塑管线,放弃部分肿瘤项目并启动裁员!
- 5药事日报227期 | 国药新冠灭活疫苗3期临床结果公布 迈瑞医疗2020年营收210.26亿......
- 6《自然》:一次用药,抗抑郁效果长达一周!胡海岚团队揭示氯胺酮长效抗抑郁分子机制
- 7克利夫兰医学中心创新峰会把脉未来2019年10大医疗科技创新
- 8德勤2018报告:医疗保健行业全景分析 亚太地区增长强劲
- 9关于辽宁省2015年医疗机构直接挂网采购药品建立配送关系的通知
- 10海南省卫生和计划生育委员会关于公布普通大输液议价结果的通知
- 11斑秃领域新药频现!
- 12精准医疗的技术基础—分子诊断技术发展现状
- 13(2017)6号关于硫酸镁注射液和重酒石酸间羟胺注射液临床紧缺药品挂网采购的通知
- 14世界十大最佳医院最新排名
- 15药事日报86期|国内新冠疫苗已经开始接种、知名药店售假口罩案终审董事长判刑15年罚款400万
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
