首款!诺华潜在重磅疗法获FDA批准
时间:2023/12/06来源:医药观澜阅读:142
诺华公司(Novartis)今天宣布,美国FDA批准Fabhalta(iptacopan)上市,作为治疗成人阵发性夜间血红蛋白尿症(PNH)的首个口服单药疗法。Fabhalta是一种补体B因子***,它在免疫系统的替代补体途径中起作用,全面控制血管内外的红细胞(RBC)**。临床试验显示,Fabhalta在大多数患者中有效提高血红蛋白水平,并且在3期临床试验APPLY-PNH中,几乎所有使用Fabhalta的患者都没有接受输血。这款药物被行业媒体Evaluate列为10款值得关注的潜在重磅疗法之一。
FDA的批准基于3期临床试验APPLY-PNH。该试验包括血红蛋白<10 g/dL且以前接受过抗C5疗法治疗但仍有残余贫血的患者。结果显示,Fabhalta在提高血红蛋白水平和避免输血方面优于继续使用抗C5疗法治疗的患者。批准还得到了3期临床试验APPOINT-PNH的支持,该研究针对未接受过补体***治疗的患者。APPLY-PNH和APPOINT-PNH试验24周的主要发现包括:
82.3%接受过抗C5疗法治疗的患者在无输血的情况下,接受Fabhalta治疗后血红蛋白水平持续增加≥2 g/dL,继续接受抗C5疗法治疗的患者这一数值为0%(P<0.0001)。未接受过补体***治疗的患者中,77.5%的患者接受Fabhalta治疗后达到了这一结果。
在无输血的情况下,67.7%接受过抗C5疗法治疗的患者血红蛋白水平持续≥12 g/dL,继续接受抗C5疗法治疗的患者这一数值为0%(P<0.0001)。
对于接受过抗C5疗法治疗的患者,接受Fabhalta治疗后避免输血率为95.2%,而抗C5疗法组患者这一数值为45.7%(P<0.0001)。
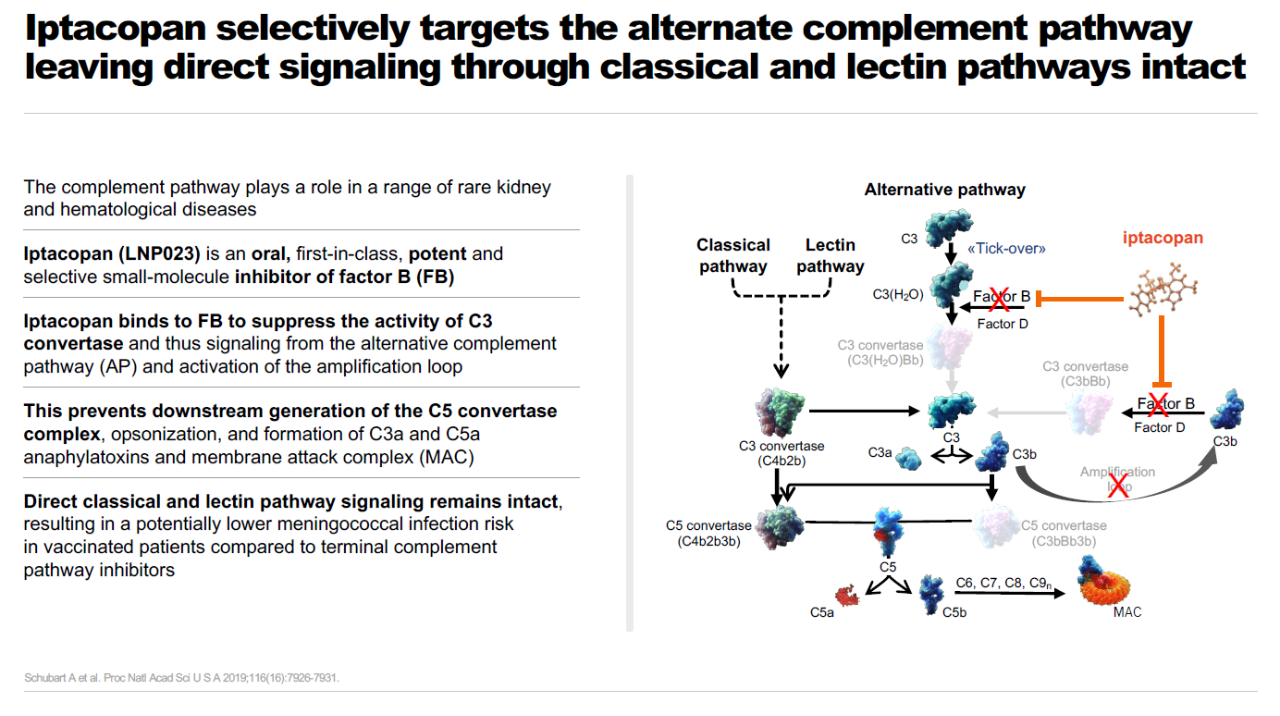
▲Iptacopan简介(图片来源:诺华公司官网)
在APPLY-PNH试验中,Fabhalta与抗C5疗法相比最常报告的不良反应(≥10%)包括:头痛(19%比3%),鼻咽炎(16%比17%),腹泻(15%比6%),腹痛(15%比3%),细菌感染(11%比11%),恶心(10%比3%)和**感染(10%比31%)。在APPOINT-PNH试验中,最常报告的不良反应(≥10%)包括头痛(28%),**感染(18%),鼻咽炎(15%)和皮疹(10%)。在APPLY-PNH中,接受Fabhalta治疗的PNH患者中有两名(3%)报告了严重的不良反应,包括肾盂肾炎、尿路感染和COVID-19。在APPOINT-PNH中,接受Fabhalta治疗的PNH患者中有两名(5%)报告了严重的不良反应,包括COVID-19和细菌性肺炎。
Fabhalta是诺华公司的重点研发项目之一,除了用于治疗PNH,它在治疗IgA肾病的3期临床试验中也已达到主要终点,预计于2024年递交加速批准的监管申请。
最新医药动态
更多»相关资讯
更多»- 1诺诚健华任命傅欣为首席财务官
- 2重磅!中国医药工业百强榜单今日揭晓!(工信部版)
- 3关于更改我中心平台相关药品信息的通知
- 4药事日报434期 | 复星医药44亿元定增方案出炉!高毅资产将成第三大股东!
- 5关于增补第二类疫苗直接挂网采购目录产品的通知
- 6尧唐生物体内基因编辑药物获批临床
- 7关于暂停部分产品长期备案采购的通知
- 8为促进临床急需境外新药审评审批 国家药监局发布最新公告
- 9跨国药企进医保太拼!诺华7款产品成大赢家 修美乐降幅83.5%
- 10临床急需境外新药标准复核检验用资料及样品有哪些要求?
- 11未来仿制药企不断洗牌和淘汰,生物药成为药代避风港?
- 12药事日报126期|辅仁被罚!实控人被罚150万元10年市场禁入、罚款83亿美元!普渡制药承认违规推广阿片类药物相关三项重罪
- 13药事日报230期 | 国家卫健委发布关于 儿童血液病、恶性肿瘤等病种诊疗规范通知......
- 14药事日报85期|华领医药与拜耳达成战略合作、万泰生物新冠病毒检测试剂盒列入WHO应急使用清单
- 15国产首款!和黄医药Syk抑制剂「索乐匹尼布」申报上市
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
