亘喜生物BCMA/CD19 CAR-T治疗RSLE的新药获批临床
时间:2023/12/25来源:药阅读:154
12月21日,亘喜生物宣布中国国家药品监督管理局(NMPA)药品审评中心(CDE)正式批准了亘喜生物旗下FasTCAR-T自体CAR-T候选疗法GC012F用于治疗难治性系统性红斑狼疮(rSLE)的新药临床试验(IND)申请。

根据此项IND批件, 亘喜生物计划在中国启动一项1/2期临床试验,以进一步评估GC012F针对rSLE患者的安全性和耐受性。
此前,亘喜生物已于11月27日宣布将在美国开展针对同适应症的1/2期临床试验。
此外,一项针对rSLE患者的由研究者发起的临床试验(IIT)正在中国开展。
GC012F是一款基于亘喜生物专有的FasTCAR次日生产平台开发的B细胞成熟抗原(BCMA)和CD19双靶点自体CAR-T候选产品。
除了即将在中美启动的两项rSLE IND临床试验外,公司已在美国开展GC012F治疗复发/难治性多发性骨髓瘤(RRMM)的1b/2期IND临床试验;
此外,还有4项IIT临床试验正在评估该疗法针对rSLE、RRMM、新确诊的多发性骨髓瘤(NDMM)以及B-NHL的临床效果。
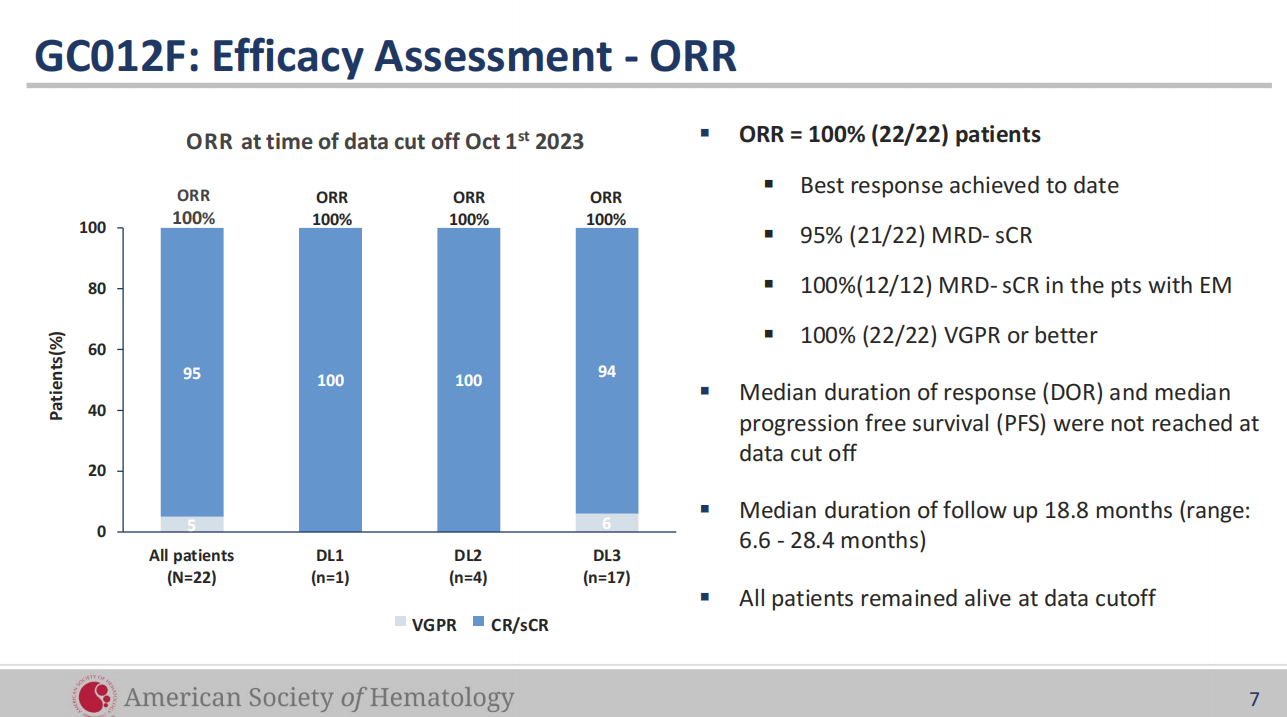
2023年11月,2023年ASH年会已公布GC012F治疗NDMM IIT临床试验的最新研究成果,该临床数据显示总体应答率(ORR)为100%,微小残留病灶阴性的严格完全缓解(MRD- sCR)率为95.5%。

亘喜生物包含多种自体和同种异体候选产品的丰富临床阶段产品管线,并有望与行业当前的CAR-T细胞疗法形成显著差异化。

最新医药动态
更多»相关资讯
更多»- 1争议:NRAS驱动癌症的新靶点——STK19
- 2美国FDA批准荣昌生物泰它西普开展治疗成人活动性原发性干燥综合征 Ⅲ 期全球多中心临床研究
- 3降血脂新药「佩玛贝特」申报上市
- 4医药快讯丨中国生物制药TQA3038完成I期临床研究;“专精特新”企业健耕医药终止科创板IPO
- 5药事日报466期 | 首个国产新冠口服药通过医保目录调整初步审查
- 6国药集团冲刺4000亿!6大上市公司战略布局曝光
- 7十方面31条!广东发布重磅文件,推进卫生健康高质量发展
- 8关于地高辛口服溶液等定点生产品种挂网采购的有关通知
- 9关于对山东省医疗机构药品集中采购临床用量小补充药品和第七批低价药品挂网公布的通知
- 10罗氏BTK抑制剂部分临床试验被FDA暂停
- 11最新!16家医械巨头营收大公开 涉迈瑞、强生、美敦力
- 127个4+7品种开启降价大风暴!12个品种新竞争者已入局
- 13药事日报345期 | 重药控股董事长辞职等多位高层变动!多项药物获批
- 14川药采联办〔2017〕5号关于公布执行2015年四川省公立医院药品集中采购双信封招标和谈判(议价)中标结果(第一批)的通知
- 152018年FDA批准 53个新药再创新高,这5款最具商业潜力
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
