药事日报431期 | 传奇生物:BCMA CAR-T上半年销售额2400万美元
时间:2022/07/22来源:医药之梯阅读:548
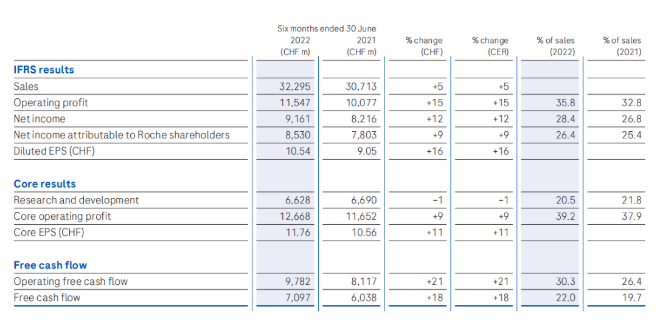
1.66亿元!迈克生物全资收购达微生物 近日,迈克生物披露半年报显示,其耗资1.66亿元完成了对北京达微生物科技有限公司(以下简称“达微生物”)100%股权的收购。 达微生物以微流控为核心技术,致力于创新型生命科学、医疗仪器和试剂的自主研发,为个体化医疗、肿瘤健康管理、基因和生命科学研究等领域提供生物医学检测仪器和应用解决方案。 早在2021年3月29日,达微生物完成了由清控金信资本领投的Pre-A轮融资,彼时迈克生物便参与跟投。具体而言,迈克生物以500万元认购达微生物3.4722%股权,同时,双方就数字PCR仪器与试剂配套开发展开战略合作。 来源:迈克生物 药明康德调高全年业绩目标:由65-70%上调至68-72% 7月21日晚间,药明康德发布2022年全年业绩目标更新公告,基于在CRDMO和CTDMO业务模式驱动下持续加速发展的信心,公司将2022年全年收入增长目标由65%-70%上调至68%-72%。 公告显示,药明康德上半年实现营业收入177.56亿元,同比增68.52%;实现归母净利润46.36亿元,同比增长73.29%;经调整非《国际财务报告准则》下归母净利润43亿元,同比增长75.68%,业绩增长创纪录。 来源:医药魔方 第8款国产PD-1获批 今日(7月22日),据国家药监局政务服务门户药品批准证明文件待领取信息显示,乐普生物抗PD-1抗体普特利单抗注射液的上市申请已获得批准,获批适应症为适用于既往接受一线及以上系统治疗失败的微卫星高度不稳定(MSI-H)/错配修复功能缺陷(dMMR)实体瘤患者的治疗。 来源:国家药监局 北大医药奥氮平片获批上市 近日,北大医药(000788.SZ)公布,公司收到国家药品监督管理局核准签发的《药品注册证书》,药品通用名称为奥氮平片。并表示,上述产品的获批,进一步完善了公司在精神类疾病领域的产品结构,有利于提升公司在精神类疾病领域产品市场的竞争力,对公司未来业绩的提升有积极作用。 来源:北大医药 飞检发现严重缺陷,一企业责令暂停生产! 7月20日,国家药品监督管理局官网发布了一则关于组织检查组对四川拜阿蒙生物活性材料有限责任公司进行了飞行检查的通知。 检查发现该企业质量管理体系主要存在以下缺陷: 企业有位于成都市望江路的生产场地A区和位于成都市高新区西芯大道的生产场地B区。现场检查发现,B区的生产场地、机构和人员、生产和检验设备属于另一关联公司。B区生产现场的设备操作规程、作业指导书等文件均为关联公司制定,企业在A区、B区的程序文件、制度文件存在两个不同版本;企业B区微生物室使用普通空调接高效过滤器的方式对空气进行净化,使用小型可移动式臭氧发生器进行室内环境消毒。 以上不符合《医疗器械生产质量管理规范》和《医疗器械生产质量管理规范附录植入性医疗器械》(以下简称《规范》)中下列要求:一是企业应当配备与生产产品相适应的专业技术人员、管理人员和操作人员,具有相应的质量检验机构或者专职检验人员;二是企业应当配备与产品生产规模、品种、检验要求相适应的检验场所和设施;三是企业应当配备与所生产产品和规模相匹配的生产设备、工艺装备等,并确保有效运行。 二、采购管理方面 企业未与B类、C类物料供应商签订质量协议,采购控制程序未对不同类别物资是否签订质量协议予以明确,不符合《规范》中企业应当与主要原材料供应商签订质量协议,明确双方所承担的质量责任的要求。 企业未能提供灭菌确认报告,不符合《规范》中灭菌过程应当按照相关标准要求在初次实施前进行确认,必要时再确认,并保持灭菌过程确认记录的要求。 来源:国家药品监督管理局 人福医药1类新药「瑞马唑仑」新适应症获批上市 7月22日,人福医药1类新药注射用苯磺酸瑞马唑仑新适应症获得国家药监局批准上市。根据临床试验进展,推测适应症为:支气管镜诊疗镇静。这是该产品上市的第3项适应症。 瑞马唑仑是一种新型的超短效静脉注射苯二氮卓类镇静药,由德国Paion公司开发。2012年,该公司以300万欧元以及后续销售分成的协议将瑞马唑仑的中国开发权益授权给人福医药。2016和2017年,Paion公司先后将瑞马唑仑的美国和日本开发权益授权给Cosmo公司和萌蒂制药。 来源:中国**采购网 罗氏2022H1业绩:总收入323亿瑞士法郎 7月21日,罗氏公布2022年上半年财报,总营收322.95亿瑞士法郎,同比增长5%(按CER计算);净利润为91.61亿瑞士法郎,同比增长12%;研发投入66.28亿瑞士法郎,与去年同期基本持平。 罗氏的收入主要来源于制药和诊断两大块业务。制药业务上半年收入223亿瑞士法郎,同比增长3%,其中中国区为16.18亿瑞士法郎(-7%);诊断业务收入99亿瑞士法郎,同比增长11%,中国区12.98亿瑞士法郎(+2%)。这主要得益于新冠肺炎相关产品销售额的增长和新上市创新药产品的亮眼表现。 来源:医药魔方 传奇生物:BCMA CAR-T上半年销售额2400万美元 2022年7月22日,金斯瑞发布公告,传奇生物BCMA CAR-T新药Carvykti上半年销售额为2400万美元。 根据协议,传奇生物拥有Carvykti大中华区70%权益,拥有海外50%权益。 2022年2月28日,FDA正式批准传奇生物/强生的BCMA CAR-T疗法Ciltacabtagene autoleucel上市,用于治疗复发性/难治性多发性骨髓瘤,商品名为Carvykti。 来源:医药笔记

一、机构与人员、厂房与设施和设备方面
三、生产管理方面
该企业质量管理体系存在严重缺陷,不符合《医疗器械生产质量管理规范》《医疗器械生产质量管理规范附录植入性医疗器械》相关规定。该企业已对其质量管理体系存在的上述缺陷予以确认。
四川省药品监督管理局应当按照《医疗器械监督管理条例》第七十二条规定,对企业依法采取暂停生产的控制措施,对涉及违反《医疗器械监督管理条例》及相关规定的,应当依法处理;并责令该企业评估产品安全风险,对有可能导致安全隐患的,按照《医疗器械召回管理办法》的规定召回相关产品。
该企业完成全部项目整改并经四川省药品监督管理局复查合格后方可恢复生产。

最新医药动态
更多»相关资讯
更多»- 12018年政府信息公开工作年度报告,48个新药上市,4个停产
- 22019海盐县人民医院最新招聘信息
- 3药事日报484期 | 阿斯利康/牛津大学鼻喷新冠疫苗I期临床失败!万泰生物2022前三季度净利润增速超200%
- 410亿美元经典降压药!花园药业缬沙坦氨氯地平片(Ⅰ)获批上市
- 52020年全国药品集采将全面发力 窗口期就要临近!
- 6国家卫健委官宣:医院次均门诊药费三年内首增长
- 7药事日报494期 | 渤健2022Q3发布!诺华天价药第3季度业绩下滑!
- 8宣泰医药 “泊沙康唑肠溶片”获加拿大卫生部批准上市
- 9苦尽甘来,眺望2023医药
- 10药事日报134期|韩国已有88人接种流感疫苗后死亡政府仍未考虑叫停 、药明巨诺正式在港交所上市
- 112019自贡市第一人民医院最新招聘信息!(急聘)
- 12药明巨诺 | 「瑞基奥仑赛注射液」新适应症上市申请获NMPA受理
- 13药事日报406期 | 万春医药宣布多位董事会成员变动;沃森生物子公司终止重组EV71疫苗研发
- 14阿斯利康创新酶替代疗法在中国获批临床
- 15K药斩获新适应症!中位OS长达12.7个月,胆道癌患者迎来免疫治疗新选择
 扫一扫关注医药之梯微信二维码
扫一扫关注医药之梯微信二维码
 个人登录
个人登录  企业登录
企业登录 
